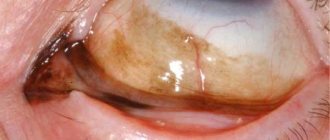
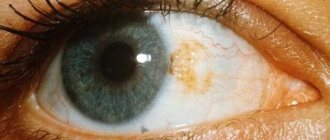
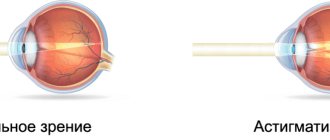
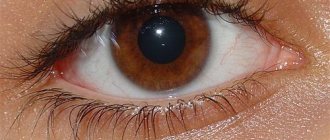
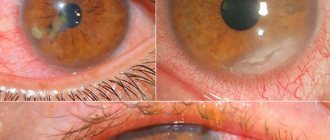
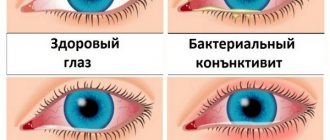
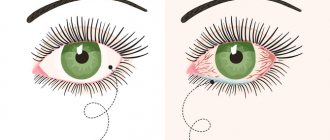
ГЛАУКОМА — хроническое заболевание глаза, при котором повышается внутриглазное давление (ВГД) и поражается зрительный нерв. При этом зрение снижается, вплоть до наступления слепоты. Слепота, вызванная глаукомой, носит необратимый характер, так как погибает зрительный нерв.
Вернуть зрение ослепшему в этом случае больному уже невозможно!
Всесторонний и индивидуальный подход к тактике ведения пациента, современные методы лечения глаукомы, предлагаемые в нашей клинике, позволяют сохранить зрение и улучшить качество жизни больным, страдающим этим заболеванием.
На сегодняшний день убедительно доказано, что чем раньше выполняется хирургическое лечение глаукомы, тем стабильнее и качественнее сохраняется зрение у пациентов!
Поэтому нами успешно применяют качественно новые методы лечения глаукомы — эффективные, безопасные и малотравматичные хирургические операции. Современная высотехнологичная хирургия глаукомы в настоящее время подразделяется на: лечение глаукомы лазером и микрохирургическое лечение глаукомы.
Лечение глаукомы лазером
Хирургия глаукомы имеет несомненные успехи, однако, становится очевидным, что как бы ни были велики достижения в технике микроманипуляций, как бы ни было мало по размерам режущее лезвие, все же даже максимальный потенциал его возможностей несоизмерим с задачей исправления патологии микроструктур тончайшей по строению фильтрующей зоны глаза. В связи с этим неизбежно встает вопрос о поисках путей «безножевой» микрохирургии глаукомы.
Уникальные возможности для этого представляет собой лазерный луч, с помощью которого можно производить операции на оболочках и внутри глаза, не вскрывая его полость, т.е. без разреза стенки. Лазерная операция при глаукоме выполняется с помощью медицинского лазера. Луч лазера может быть сфокусирован в точечное световое пятно, которое играет роль «лазерной иглы» или «лазерного ножа».
ЛАЗЕРНОЕ ЛЕЧЕНИЕ ГЛАУКОМЫ БЕЗБОЛЕЗНЕННО, НЕПРОДОЛЖИТЕЛЬНО И ПРОВОДИТСЯ АМБУЛАТОРНО, ПОЗВОЛЯЕТ ИЗБЕЖАТЬ ХИРУРГИЧЕСКОГО ВМЕШАТЕЛЬСТВА НА ГЛАЗНОМ ЯБЛОКЕ.
Лечение глаукомы лазером в отличие от хирургической операции не требуется общей анестезии, может быть выполнено в амбулаторных условиях при минимальной длительности послеоперационного освобождения от работы. Поскольку лазерная операция при глаукоме производится без вскрытия глаза, она не сопровождается теми осложнениями, которые могут возникнуть во время и после антиглаукоматозных микрохирургических операций. Лазерное лечение глаукомы имеет весьма существенное достоинство — восстановление оттока внутриглазной жидкости (ВГЖ) по естественным каналам.
Тракционные лазерные операции
В настоящее время широко распространенными и наиболее эффективными являются лазерные методы лечения глаукомы, основной зоной воздействия которых является трабекулярная сеть угла передней камеры. Такое лазерное лечение глаукомы называется тракционная лазерная операция и заключается в нанесении лазерокоагулятов в зоне трабекулы, что приводит к расширению трабекулярных щелей и увеличению оттока внутриглазной жидкости из глаза.
Сегодня антиглаукоматозные лазерные операции подобного типа прекрасно зарекомендовали себя при открытоугольной глаукоме. Наиболее часто используются следующие: линейная и радиальная лазерная трабекулопластика, передний и задний трабекулоспазис, циклотрабекулоспазис.
1 – лазерная трабекулопластика
2 – передний трабекулоспазис
3 – задний трабекулоспазис
4 – циклотрабекулоспазис
После лазерных операций рекомендуется в течение некоторого времени (до 2-х недель) продолжать принимать те гипотензивные средства, которые пациент получал до вмешательства. Для уменьшения выраженности реактивного синдрома и послеоперационной воспалительной реакции местно (в виде капель) назначаются противовоспалительные препараты. После исчезновения симптомов реактивного воспаления дозы гипотензивных средств постепенно уменьшаются или отменяются полностью.
OPHTHALMO.RU
Предыдущий форум, состоявшийся в Вене два года назад, объединил различные глаукомные общества всего мира. Именно тогда членом данной организации стало Российское глаукомное общество. Теперь AIGS прекращает свое существование, превращаясь в организацию мирового уровня, которая будет называться – World Glaucoma Association (WOG) и первым форумом ее будет конгресс в Бостоне (США) в 2009 г.
Целью международной организации глаукомных обществ является не только объединение ведущих мировых ресурсов и наиболее значимых исследований по проблемам глаукомы, но и повышение образовательного уровня всех глаукоматологов мира. Другая немаловажная цель – достижение консенсуса по вопросам диагностики и лечения глаукомных больных. Эти задачи решаются в процессе работы международных конгрессов, которые вот уже на протяжении более десяти лет проводятся в разных точках земного шара каждые два года.
Конгресс в Сингапуре, собравший около 2 тыс. участников, проходил в крупном выставочном центре (Конгресс-холл Сантек-Сингапур) при поддержке и широком участии ведущих фармацевтических фирм и компаний по производству медицинской техники. В работе приняли участие офтальмологи со всего Земного шара. В числе докладчиков были ведущие специалисты, как из США, так и Европейских стран. Надо отметить, что среди участников конгресса было значительное количество офтальмологов из стран Азии.
За день до открытия конгресса 17 июля Институтом последипломного образования США был устроен симпозиум “Последние достижения в нейропротекциии при глаукоме”. Симпозиум был организован при поддержке компании Allergan.
Во вступительном слове д-р R.Weinreb (США) обосновал необходимость поиска нейропротекторной терапии, подчеркнув, что в течение 20 лет 27% больных глаукомой становятся слепыми на один глаз и 9% слепнут на оба глаза, причем, если на фоне гипотензивного лечения больные слепнут в 4.4%, то при отсутствии лечения – в 9%. Оценить эффективность нейропротектороного лечения – весьма непростая задача, поскольку результат от подобного вида терапии наступает гораздо позднее, чем непосредственный эффект от местных гипотензивных препаратов.
Обсуждая механизмы развития ГОН M.Rosarioo Hernadez (США) особое внимание обратил на взаимодействие ганглиозных клеток сетчатки и глии. Астроциты, представляя глиозную ткань сетчатки, в норме принимают активное участие в процессах ремоделирования ткани, замещая погибшие аксоны. При глаукоме астроциты, продуцирующие факторы роста и различные химические субстанции, нарушают нормальное окружение аксонов, приводя к их гибели. Триггерным механизмом в этом случае может выступать непосредственно повышенное ВГД. Наряду с астроцитами Мюллеровы клетки сетчатки, также представляющие глиозную ткань, регулируют процессы захвата ганглиозными клетками сетчатки нейротрансмиттеров, в т.ч. глутамата и регулируют ионный гомеостаз ГКС. Значение Мюллеровых клеток в патогенезе ГОН изучена значительно меньше, чем астроцитов, которым отводят ключевую роль в механизмах гибели аксонов и тел ГКС.
Примечательно, что наиболее ранние патологические механизмы при глаукоме развиваются в митохондриях аксонов и заключаются они в активации окислительного стресса, структурном повреждении митохондрий, активации их энзимов и апоптоза клеток. Полагают, что именно митохондрии аксонов ГКС являются точкой приложения раннего нейропротекторного лечения.
Интересным было сообщение д-ра N.Gupta (Канада), которая подчеркнула, что глаукома – это нейродегенеративное заболевание не только зрительного нерва, но всего зрительного анализатора. Посмертные исследования головного мозга больных глаукомой выявили изменения в хиазме, наружных коленчатых телах, зрительной лучистости и даже в зрительной коре. Автор делает вывод о том, что в тот момент, когда у больных глаукомой обнаруживаются изменения в полях зрения, снижающие светочувствительность сетчатки в два раза, уже имеются поражения центральной нервной системы (цнс). Доклад д-ра N.Gupta вызвал бурные обсуждения. В результате дискуссии участники пришли к выводу, что в скором времени по изменениям, выявленным в цнс (например, в ходе магнитно-резонансной томографии), можно будет диагностировать глаукому. Интересен вопрос о том, что является первичным поражением при глаукоме – гибель нейронов в зрительной коре или в сетчатке. По этому поводу также разгорелась дискуссия. N.Gupta считает, что первично поражение цнс, однако доказать это мы пока не в силах.
Немало сообщений на этом заседании было посвящено оценке скорости прогрессирования глаукомной оптиконейропатии (ГОН). Действительно, это – не простая задача. Оказывается, оценивая прогрессирование ГОН по периметрическому индексу MD, мы убеждаемся , что эта скорость составляет 0,9 dB год, и только в 10% случаев – более, чем 1.5 dB год. По данным A.Heijl (Швеция), при исходном индексе MD -4,0 dB за пять лет ухудшение индекса до -20 dB происходит только у пятой части больных. В два раза выше скорость прогрессирования при псевдоэксфолиативной глаукоме. Примечательно, что местное гипотензивное лечение, как правило, более эффективно снижает ВГД, но гораздо менее влияет на уровень изменения индекса MD. Вывод из этих наблюдений прост – глаукома прогрессирует несмотря на нормализацию ВГД, причем наиболее важный фактор прогрессирования – уже имеющееся глаукомное поражение (чем ниже исходный индекс MD, тем быстрее прогрессирование). Во всех случаях быстрого прогрессирования ГОН рекомендуется проводить периметрию каждые три-четыре месяца.
Каковы же реальные нейропротекторы, которыми мы располагаем в настоящее время? Примечательно, что на данном симпозиуме упоминались лишь два из них, причем только один применяется в настоящий момент в практике. Речь идет об α2-адреномиметике бримонидине . Учеными из США ( Wheeler L., Hare W.) было показано, что приток ионов кальция внутрь клетки успешно подавляется бримонидином. C.Girkin (США) в своем исследовании на культуре ГКС продемонстрировал защитную функцию бримонидина, который повышает выживаемость клеток в условиях транзиторной ишемии
Блокада глутамат-кальциевого каскада осуществляется также мемантином. Это – еще один нейропротектор, обсуждаемый широко на данном симпозиуме. Оба препарата (бримонидин и мемантин) действуют по дозо-зависимому пути и на сегодня являются наиболее перспективными нейропротекторами.
Рассматривая перспективы применения блокатора NMDA-рецепторов мемантина, д-р A.Lipton (США), подчеркнул, что за последние годы были потрачены огромные средства на исследования различных блокаторов NMDA-рецепторов в лечении ГОН, однако ни одно из них не увенчалось успехом в силу чрезвычайной токсичности применяемых препаратов. Важно отметить, что д-р A.Lipton является ведущим нейробиологом мира, который внес большой вклад в разработку методов лечения нейродегенеративных заболеваний, в частности б-ни Альцгеймера. Его исследования, особенно, в области применения мемантина при заболеваниях цнс, были отмечены высокими наградами в США.. A.Lipton обратил внимание офтальмологов, что для получения нейропротектороного эффекта при ГОН требуются очень небольшие дозы мемантина (какие именно, пока не известно!). Передозировка приведет к обратному действию – к активации NMDA-рецепторов. Вот почему на сегодня данный препарат не разрешен в США к применению при глаукоме, оставаясь однако одним из наиболее перспективных в будущем нейропротекторном лечении ГОН.
Напомним, что целью лечения глаукомы, согласно рекомендациям европейского глаукомного общества и мировым стандартам, является как можно более длительное удержание на должном уровне качества жизни больных. Это подразумевает не только сохранение зрительных функций (их уровень оценивается, главным образом возможностью управлять автомобилем), но также учитываются экономические и социальные аспекты, т.е. какой ценой достигается это сохранение полей зрения. Следует подчеркнуть, что вопросам качества жизни был посвящен целый симпозиум, на котором офтальмологи пришли к заключению, что качество жизни при глаукоме страдает гораздо раньше, чем это было принято считать раньше. Доктором A.Viswanathan (Великобритания) было подчеркнуто, что это происходит между переходом глаукомы из начальной стадии в развитую: у 71% больных уже в начальную стадию заболевания возникают проблемы, связанные с управлением автомобиля. Д-р R.Hitchings (Великобритания) предложил для оценки качества жизни б-х глаукомой, а именно для определения их возможностей управлять автомобилем, оценивать интегральные поля зрения, т.е. результаты наложения данных периметрии обоих глаз. Им было показано, на сколько подобный подход информативнее отражает уровень повреждения зрительных функций.
Интересно, что нейропротекторное лечение, по мнению большинства докладчиков, более показано пациентам с так называемой ВГД-независимой глаукомой. Иными словами, если прогрессирование ГОН мало связано с высоким ВГД, а более – с иными, например, сосудистыми факторами, то нейропротекторное лечение будет ведущим терапевтическим методом. Порой бывает непросто отдифференцировать этих пациентов. Но видимо, этим обусловлено более или менее доброкачественное течение ГОН у разных больных: в том случае, если имеется некий механический фактор прогиба решетчатой мембраны склеры, который можно устранить путем снижения ВГД, то прогрессирование ГОН можно приостановить. Другое дело, когда ГОН определяется иными факторами, например, сосудистой дисрегуляцией, тогда на арену выходит нейропротекторное лечение, в котором ученые офтальмологи мира, как это было резюмировано в конце симпозиума, пока не слишком преуспели.
Работа самого конгресса, начавшаяся на следующий день, была построена по принципу сочетания пленарных заседаний в больших конференцзалах с тематическими симпозиумами-курсами, которые повторялись в разное время с тем, чтобы участники могли посетить как можно больше интересующих их мероприятий. Новым в организации конгресса было проведение так называемых дебатов, список которых был разослан задолго до начала конгресса, с тем чтобы участники могли определиться с наиболее интересными темами. Во время дебатов ведущие специалисты обсуждали какую-либо проблему (например, глаукома нормального давления или что нового в хирургии глаукомы, а также глаукома как нейродегенеративное заболевание и т.д.) между собой и с присутствующими в зале. В ходе дебатов вырабатывался консенсус.
Значительное количество сообщений было посвящено закрытоугольной глаукоме (ЗУГ), что не удивительно, т.к. именно данная форма глаукомы встречается наиболее часто в Азии, где собственно и проходил конгресс. По данным H.Quigley (США) эта форма глаукомы приводит к инвалидности в большей степени, чем ПОУГ. Среди 60 млн. больных глаукомой на земном шаре 44 млн. имеют открытоугольную форму, а 16 млн. –закрытоугольную, причем последняя особенно часто встречается в Китае (в пять раз чаще, чем в других регионах земного шара)..
Весьма насыщенным было заседание, посвященное патогенезу различных форм глаукомы. Останавливаясь на механизмах развития ЗУГ, доктор D.Lam (Гонконг) обратил внимание офтальмологов на частую причину нарастающей ретенции при закрытом угле в виде адгезии корня радужки к пигментированной части трабекул. Формирование гониосинехий приводит к длительной и даже постоянной ретенции, что в конечном итоге отражается на состоянии зрительного нерва. Были сделаны некоторые замечания относительно терминологии: под острой закрытоугольной глаукомой понимается состояние, соответствующее приступу, а под хронической – заболевание, при котором в результате постоянного сужения или закрытия УПК наступает глаукомная оптиконейропатия.
Рассматривая механизмы развития закрытоугольной глаукомы, R.Ritch (США) остановился на четырех основных путях формирования ретенции: зрачковый блок, плоская радужка, закрытие УПК хрусталиком и злокачественная глаукома. Автор подчеркнул важное значение гониоскопии, которая позволяет отдифференцировать функциональный блок от органического (имеются синехии). Особое внимание обращено на форму ЗУГ с плоской радужкой. Диагноз наиболее точно в этом случае ставится по данным ультразвуковой биомикроскопии, когда выявляется мелкая задняя камера, что в принципе не характерно для ЗУГ. В этом случае докладчики настоятельно рекомендовали выполнять периферическую иридопластику.
Большое внимание было уделено современным методам визуализации переднего сегмента глаза методом ОКТ. Вместе с тем, останавливаясь подробнее на оценке состояния УПК, D.Friedman (США), обратил внимание на недостатки каждого из существующих методов: даже наиболее информативный из них – ОКТ не позволяет визуализировать цилиарное тело, что бывает крайне необходимо для выбора тактики ведения больного с ЗУГ. При этом важно помнить, что лишь у 20% больных с закрытым углом развивается приступ глаукомы, у остальных глаукома протекает по типу хронической. Quigley H подчеркивает, что только у одного из 10 пациентов с узким УПУ развивается ЗУГ. Важную роль в этом, по мнению автора, играет состояние стекловидного тела и сосудистой оболочки.
В патогенезе ПОУГ д-р E.Tamm (Германия) особое внимание обратил на отложение экстраклеточного матрикса в юкстаканаликулярной части трабекул. Причиной данного явления считают избыточный синтез трансформирующего фактора роста ( TGF β 2).
Рассказывая о патогенезе пигментной глаукомы д-р R.Ritch (США), подчеркнул, что это – наследственное заболевание, передающееся по аутосомно-доминантному типу, и связанное с повреждением метаболизма сератонина, допамина и тирозина. Заболевание проявляется, главным образом, в третьей декаде жизни и идет на убыль по мере прогрессирования пресбиопии, т.к. наибольший выброс пигмента из пигментного листка радужки происходит во время аккомодации. Лечение пигментной глаукомы, по мнению докладчика, должно быть генетическим.
Останавливаясь подробно на механизмах развития псевдоэксфолиативной глаукомы (ПЭГ), д-р U. Schlotzer – Schrehardt (Германия), подчеркнула, что заболевание представляет собой проявление стресс-индуцированного эластоза и эласто-микрофибриллопатии, ключевыми моментами которого являются избыточный синтез TGF β 1, окислительный стресс и слабо выраженный воспалительный процесс. Докладчик обратила внимание на системный характер заболевания и подчеркнула роль нарушения глазной перфузии при ПЭГ. Было отмечено, что заболевание особо распространено среди эмигрантов из России (в самой России эпидемиология не представлена).
В патогенезе нормо-тензивной глаукомы (НТГ), по мнению M.Wax (США), многое остается неясным. Предполагают, что в основе механизмов, повреждающих сетчатку и зрительный нерв при НТГ, могут лежать как наследственные причины, так и нарушения нормальных физиологических процессов вследствие следующих предрасполагающих факторов: 1.вазоспазм, 2.сосудистая дисрегуляция, 3.морфологические нарушения склеры как, например, при миопии, 4.образование анти-фосфолипидных антител, 5.генетические повреждения, 6.апоноэ во время сна, 7.аутоиммунные механизмы. В ходе дискуссии по проблемам НТГ неоднократно подчеркивалась необходимость частого измерения ВГД, особенно в ночные часы, когда имеются пики подъема ВГД. Доктор Yamomoto отметил, что в Японии существует практика измерения ВГД и АД при обследовании больных с нормотензивной глаукомой каждые четыре часа в течение суток. Доктора из Европы при НТГ делают акцент на измерении глазной гемодинамики, что широко практикуется в Германии и Швейцарии.
Обсуждению роли ВГД в развитии и прогрессировании глаукомы было посвящено несколько заседаний. Это подчеркивает тот факт, что наши зарубежные коллеги придают серьезное значение ВГД в патогенезе заболевания, однако по-прежнему, называют его фактором риска. На данном конгрессе было сделано по крайне мере несколько важных заявлений, касающихся роли офтальмотонуса в развитии глаукомы. Во-первых, подчеркивалась важность суточной тонометрии, особенно в ночные часы, поскольку измерение ВГД в первой половине дня низко информативно. Следует отметить признание зарубежными офтальмологами ведущей роли высокого ВГД в прогрессировании ГОН. Вместе с тем, роль суточных флуктуаций ВГД в прогрессировании заболевания теперь не признается как существенный фактор риска. Если еще недавно говорили о высокой корреляции между уровнем ВГД и толщиной роговицы в ее центральной части, то теперь подчеркивается, что прямого соответствия между этими понятиями не существует, а измерение толщины роговицы наиболее важно с точки зрения риска прогрессирования ГОН (чем тоньше роговица, тем выше этот риск). И наконец, очень важное резюме было сделано относительно давления цели. Рекомендуется, рассчитывая этот показатель, базироваться на стадии глаукомного поражения, на предполагаемой оставшейся продолжительности жизни для конкретного больного (с этой целью были даже продемонстрированы графики перерасчета текущего возраста на оставшиеся годы!), а также сопутствующие факторы риска, включающие состояние парного глаза и семейный анамнез по глаукоме. Факторы риска прогрессирования ГОН (кстати, они же – факторы риска перехода офтальмогипертензии в глаукому), изученные в нескольких мультицентровых исследованиях, были обобщены на данном симпозиуме. Среди них следует отметить высокое ВГД, тонкую роговицу, большую экскавацию ДЗН (по вертикали), асимметрию ДЗН между двумя глазами, высокий периметрический индекс PSD, возраст, низкое перфузионное давление, мигрень, кровоизлияния на ДЗН, пседоэксфолиативный синдром, синдром пигментной дисперсии и несколько антиглаукомных операций в анамнезе. Примечательно, что сахарный диабет, миопия и флуктуации ВГД в настоящее время не рассматриваются как серьезные факторы риска и их роль в развитии заболевания еще предстоит выяснять.
Важное значение на данном конгрессе уделялось оценке структурных и функциональных изменений в определении скорости прогрессирования глаукомы. Анализируя литературу с 2003 г., посвященную функциональным тестам при глаукоме, D.Garway-Heath (Великобритания), подчеркнул, что стандартная автоматизированная периметрия (САП), которая наиболее часто применяется в диагностике глаукомы, неприемлема для раннего выявления заболевания. С этой целью наиболее адекватно использование сине-желтой периметрии (SWAP) или периметрии с удвоенной частотой (FDT). Однако анализ литературы показал, что трудно выявить преимущества одного из указанных селективных методов функциональной диагностики. Идеальным из них можно считать тот, который обладает высокой воспроизводимостью, позволяет выявлять ранние нарушения светочувствительности и, что не мало важно, прост в выполнении и легко переносится больным.
Подчеркивая важность исследования структурных изменений при глаукоме, L.Zangwill (США) базировался на положениях, разработанных AIGS: 1.Методы структурных исследований при глаукоме должны войти в рутинную практику офтальмолога, 2.Цветное стерео-фотографирование ДЗН является наиболее важным методом оценки состояния ДЗН при глаукоме. 3.Дополнительные методы с применением цифровых технологий и сопутствующей базы данных являются весьма полезными в оценке прогрессирования заболевания. 4.Применение нескольких компьютерных методов оценки структурных изменений ДЗН и слой нервных волокон сетчатки (СНВС) позволяют наиболее точно оценить стадию заболевания.
Интересное исследование было выполнено офтальмологами Индии, которые изучали влияние физических упражнений (включая занятие йогой) на ВГД. Оказалось, что умеренные физические нагрузки существенно понижают офтальмотонус. Однако при занятии йогой в положении на голове, равно как и при подъеме тяжестей, а также атлетических упражнениях ВГД поднимается. Кратковременное повышение офтальмотонуса наблюдается при психическом стрессе. Авторы рекомендуют учитывать полученные результаты и рекомендовать больным глаукомой применять местные гипотензивные препараты при занятиях спортом, например, закапывать пилокарпин при пигментной глаукоме.
Много сообщений было посвящено молекулярным механизмам патогенеза глаукомы. Особого интереса заслуживали доклады, посвященные генной терапии. Доктор T.Borras (США) доложила о результатах идентификации генов, ответственных за процессы физиологии и патофизиологии трабекулярной сети, а также — о способах доставки генных препаратов непосредственно к зоне трабекул при помощи адено-вирусного вектора. Среди идентифицированных генов были названы кальдесмон, тропомиозин (гены, ответственные за формирование дренажной зоны), процессы кальцификации (остеоглицин, матрикс- Gla), белки, защищающие от стресса (миоциллин, αβ-коисталлин) и сигнальные нейропептиды (субстанция Р, секретогранин). Интересно, что поиск генных препаратов идет в направлении лекарств, усиливающих отток внутриглазной жидкости. Преимущества генной терапии заключаются в ее большей эффективности и значительно меньшей токсичности по сравнению с традиционным лечением, что обусловлено избирательным действием генных препаратов.
Если первые два дня конгресса были посвящены проблемам эпидемиологии, диагностики и патогенеза различных форм глаукомы, то следующие два дня – проблемам лечения. В частности большое внимание было уделено выбору тактики ведения больных. Очевидно, она носит индивидуальный характер, однако принципиально важно решить, с чего начинать лечение впервые выявленной глаукомы: с назначения капель, или с лазерного лечения? Мнения по этому поводу разделились. Сторонники лазерного лечения как первого этапа терапии, ссылались на большую эффективность этого метода: больной не пропускает закапывания капель, т.к. в ряде случаев они ему просто становятся не нужны. Тем не менее аргон-лазерная трабекулопластика вызывает рубцевание структур УПК. Это было основным доводом сторонников медикаментозного лечения. Против этого мнения был выдвинут аргумент, что современный вид трабекулопластики – СЛТ является весьма щадящим и вместе с тем эффективным методом. Тем не менее в развитых странах лечение глаукомы традиционно начинают с назначения местных гипотензивных закапываний, и как правило, речь идет о монотерапии. Вместе с тем замечено, что спустя два года 49-75% больных нуждаются в назначении дополнительных капель, и тогда стоит серьезно задуматься о назначении фиксированных комбинаций препаратов. Таким препаратам, как косопт, комбиган (к сожалению, в нашей стране до сих пор нет этих препаратов), ксалаком и проч. было посвящено несколько сообщений. Соронники назначения фиксированных комбинаций препаратов утверждают, что они дают меньше побочных действий (видимо, за счет уменьшения концентрации консерванта бензалкония). Однако, сложнее бывает установить, какая именно составляющая применяемой комбинации эффективна, а какая – нет.
Серьезной проблемой является лечение глаукомы в развивающихся странах. В докладе “Роль циклодеструкции в лечении глаукомы в третьем мире” H.Quigley высказал сомнение по поводу того, что диодная циклокоагуляция может решить проблему там, где недоступна хирургия. Автор подчеркивает, что хотя выполнение диодной циклокоагуляции и не требует высокой техники, тем не менее исследования отдаленных последствий этой процедуры в странах третьего мира носят весьма ограниченный характер и результаты этих исследований не слишком утешительны (только в двух третях случаев удается достичь снижения ВГД до 22 мм рт.ст. И это – после проведения нескольких процедур). Как альтернативную меру автор предлагает выполнение лазерной трабекулопластики. Что касается диодной циклокоагуляции, то этот метод более показан больным с рефрактерной глаукомой.
Сравнивая эффективность двух методов лазерной трабекулопластики – аргоновой и селективной, R.Ritch подчеркнул, что они оба одинаково эффективны, с той лишь разницей, что СЛТ более эффективна у пожилых пациентов и может быть повторена, в этом – ее преимущество, однако результаты СЛТ при вторичных глаукомах еще предстоит изучать. Автор подчеркнул низкую эффективность лазерной трабекулопластики у молодых пациентов, особенно при миопии высокой степени.
По-прежнему неоднозначно решается вопрос о целесообразности выполнения периферической лазерной иридэктомии при закрытом угле передней камеры. Д-р Thomas (Индия) изложил результаты консенсуса по этому вопросу: процедура показана во всех случаях при приступе закрытоугольной глаукомы, в т.ч. и для профилактики приступа на парном глазу. В то же время известно, что около 8% населения имеют узкий или закрытый УПК (что проявляется при гонисокопии, когда УПК закрыт на 180 градусов при выполнении специфических тестов). Тем не менее данное состояние в большинстве случаев имеет доброкачественное течение и переходит в хроническую закрытоугольную глаукому в течение пяти лет лишь в 22% случаев, как правило, не приводя к слепоте. Поэтому показания к профилактической иридэктомии в таких случаях относительны. Важнее, по мнению автора, вовремя определить факторы риска развития ЗУГ и принять своевременные меры.
На видеосессии, посвященной хирургии, большое внимание было уделено сочетанной хирургии, причем авторы неоднократно подчеркивали, что вопрос о выборе тактики последовательной или одномоментной хирургии катаракты и глаукомы во всех случаях решается индивидуально. Рассматривались такие детали хирургической техники, как выбор ИОЛ при факотрабекулэктомии, сохранение конъюнктивального и склерального лоскутов, имплантация ИОЛ при разрывах задней капсулы и цинновых связок, а также при узком зрачке. Следует подчеркнуть, что по-прежнему очень большое внимание за рубежом уделяется применению антиметаболитов (главном образом, митомицина С) в предупреждении избыточного рубцевания. Выбору доз и технике применения ММС было посвящено не одно заседание. Khaw (Великобритания) отметил преимущества техники с использованием punch в выполнении синустрабекулэктомии, подчеркнув меньший риск развития послеоперационной гипотонии. При этом автор настаивал на плотном ушивании склерального лоскута. Интересным было обсуждение вопроса о том, что делать в случае неудачной антиглаукомной операции. Вопрос о том, выполнять ли ревизию предыдущей зоны, делать антиглаукомную операцию в новом месте или перейти к лазерной циклодеструкции, периодически возникает перед любым хирургом-глаукоматологом. Доктор A. Manda (Канада) считает, что предпочтение в этом случае следует отдать хирургии в новом месте, причем с использованием ММС или дренажа. Лазерная циклодеструкция показана при низких зрительных функциях пациента.
Подводя итоги прошедшего форума, следует отметить, что акценты проводимых исследований, в том числе и перспективных, делаются на нейропротекторном лечении глаукомы. Именно поэтому наиболее важные из этих исследований (в частности, в области применения мемантина и доставки лекарств методом аденовирусного вектора) были отмечены наградами и мировым признанием. Заслуживает сожаления скромное участие российских офтальмологов в процессе развития мировой глаукоматологии.
Отчет подготовила профессор Н.И.Курышева
Транссклеральная лазерная циклокоагуляция
В данном случае лазерное лечение глаукомы заключается в термической деструкции части цилиарного тела с целью снижения продукции водянистой влаги и внутриглазного давления.
Показания к этому методу лазерного лечения:
- первичная глаукома в далекозашедшей стадии, не поддающаяся традиционным методам лечения,
- терминальная глаукома при некупируемом традиционными методами лечения болевом синдроме,
- сосудистая офтальмогипертензия и глаукома, независимо от стадии процесса (посттромботическая после острой непроходимости центральной вены сетчатки, неоваскулярная после острой окклюзии центральной артерии сетчатки, геморрагическая после рецидивирующих гемофтальмов),
- диабетическая неоваскулярная дегенеративная глаукома,
- посттравматическая глаукома и офтальмогипертензия (в том числе постожоговая).
Подготовка пациента и этапы лазерной циклокоагуляции глаз
Перед осуществлением рассматриваемой манипуляции доктор проводит визуальный осмотр пациента, а также назначает комплекс диагностических мероприятий:
- Проверка остроты зрения.
- Компьютерная рефрактометрия для выявления факторов, спровоцировавших ухудшение зрения.
- Биомикроскопия позволяет оценить состояние компонентов глазного яблока.
- Офтальмоскопия. Дает возможность изучить глазное яблоко изнутри; протестировать структуру диска зрительного нерва.
- Бесконтактная тонометрия для ежедневного измерения ВГД. Перед хирургическим вмешательством пациенту назначают препараты, благоприятствующие нормализации внутриглазного давления.
- Исследование при помощи УЗИ-аппарата, оптическая томография – дополнительные методы диагностики, которые могут быть назначены в отдельных случаях.
За пару дней до лазерной циклокоагуляции проводят проверку общего состояния здоровья пациента, которая включает:
- Общий анализ крови и мочи.
- Биохимическое тестирование крови.
- ЭКГ.
Алгоритм выполнения операции следующий:
- Местное обезболивание. Зачастую используют инъекции Лидокаина. Действие анестетика наступает через 7-10 минут.
- Нанесение лазерных коагулятов на область стыковки склеры с роговой оболочкой.
Чаще всего выбор делают в пользу транссклерального метода. Он несложный и малоинвазивный, однако здесь существует высокая вероятность повреждения близлежащих тканей. Чуть реже применяют транспупиллярный способ визуализации. Оперирующий может дозировать влияние на цилиарные отростки, обеспечивая высокую результативность процедуры. Однако указанная методика чревата высоким риском развития обострений в будущем. Еще одна методика проведения лазерной циклокоагуляции – эндоскопическая. C ее помощью хирург способен полностью следить за ходом операции. В силу технической сложности данный метод не является распространенным на сегодняшний день. - Лазер устанавливается с начальной мощностью 1750 мВт и длительностью 2 секунды. Если по истечению указанного периода не было щелчка («поп») изнутри глаза, мощность повышают. После того, как будет слышен «поп», мощность снижают каждый раз на 250 мВт, пока специфический звук не исчезнет вовсе. Расстояние между лазерными коагулятами составляет около 2 мм.
В том случае, если требуется повторное хирургическое вмешательство, его проводят не ранее чем через 3-4 недели после первой лазерной циклокоагуляции.
Лазерная иридэктомия (иридотомия)
| Показания к лазерной иридэктомии такие же, как и к хирургической. Лазерная иридэктомия применяется при первичной и вторичной закрытоугольной глаукоме, при смешанной глаукоме. Лазерная иридэктомия показана как дополнительное вмешательство после внутриглазных операций при неполной эксцизии радужки или закрытии ее колобомы спайками и пигментом. С профилактической целью лазерная иридэктомия может быть выполнена на втором глазу при первичной односторонней закрытоугольной глаукоме и как предварительный этап перед трабекулопластикой на глазах с открытоугольной глаукомой и узким углом передней камеры. Лазерная иридэктомия противопоказана при отеке и помутнениях роговицы и при мелкой передней камере. |
Лазерная транссклеральная циклофотокоагуляция при глаукоме. Цена в Москве
Циклофотокоагуляция, также называемая специалистами циклотерапией или циклоиссечением, является широко применяемым методом лечения сложных заболеваний глаз. Метод назначается в случае незрячего глаза, с постоянным болевым синдромом и при конечной терминальной стадии глаукомы.
Транссклеральную циклофотокоагуляцию считают последним аргументом офтальмолога в случае, если иные методики борьбы с заболеванием не приносят должного эффекта, а использовать необходимые группы препаратов не представляется возможным и речь идет о сохранности глаза.
Суть метода транссклеральной циклофотокоагуляции
Главной задачей процедуры циклофотокоагуляции является снижение объема жидкости, находящейся в глазной полости. Достигается это хирургическим путем, с частичным разрушением производящего влагу цилиарного тела.
В недалеком прошлом, когда офтальмологические лазеры были только мечтой специализированных клиник, воздействие на цилиарное тело пытались проводить методом электродиатермии (электролечение) либо сеансами криотерапии. Правда, подобные попытки имели слабый терапевтический эффект и не позволяли контролировать объем искусственно разрушаемой ткани.
Зачастую, такие деструктивные воздействия вышеназванных процедур приводили к нежелательным последствиям, когда нормальная жизнедеятельность глаза ставилась под угрозу из-за утраты необходимого количества влаги.
В отличие от прежних вариантов, транссклеральная циклофотокоагуляция является во много раз более точным малоинвазивным методом. При этом, ее проведение обходится практически без осложнений — разрушения и инфицирования подвергшихся операции тканей.
Такие положительные стороны процедуры циклофотокоагуляции являются причиной, по которой ее назначают пациентам с высоким уровнем ВГД. Ведь у этой категории больных часто отмечаются сильный болевой синдром, приводящий к повреждению зрительного нерва и полной утрате зрительных функций.
Виды и типы циклофотокоагуляции
Современная офтальмология может предложить целый ряд методов, которые дают возможность наладить выработку требуемого объема внутриглазной жидкости. При этом, процедуру циклодеструкции принято подразделять на отдельные методы:
- Циклокриотерапию, способ воздействия жидким азотом, применяемый достаточно редко;
- Контактную трансклеральную циклофотокоагуляцию, когда для воздействия используют полупроводниковый G-зонд контактного лазерного;
- Бесконтактную транссклеральную циклофотокоагуляцию, в которой применяется неодимовый АИГ-лазер;
- Эндоскопическую циклофотокоагуляцию.
Вариант эндоскопической циклодеструкции, или эндоциклофотокация, нередко оказывается более предпочтительной в сравнении с прочими методами. Ее можно выполнять, как самостоятельную процедуру или совмещать с хирургическим лечением катаракты.
Процедура подразумевает введения в глаз специального щупа, снабженного микролазером с источником света. Перемещая щуп вокруг радужки, хирург-офтальмолог оценивает состояние цилиарного тела. Затем следует воздействие лазером, после которого, жидкость вырабатывается лишь сохранившейся частью клеток цилиарного тела.
Для выполнения операции применяется, как диодный, так и неодимовый лазеры.
Показания и противопоказания циклофотокоагуляции
Показанием к проведению операции транссклеральной циклофотокоагуляции служат следующие заболевания и состояния глаз:
- Терминальная стадия любого вида открытоугольной глаукомы (неоваскулярной, травматической, первичной и вторичной).
- Последствия неудачной кератопластики.
- Болящий незрячий глаз.
Противопоказаниями к проведению процедуры называют выраженные проявления увеита, злокачественные новообразования в области дистального отдела глаза, нормальную остроту зрения.
Периферическая иридопластика и пуппиллопластика
Иридопластика (гониопластика, иридоретракция) заключается в нанесении на периферии радужки легких лазерных коагулятов. Сморщивание и ретракция стромы радужки приводят к немедленному расширению угла передней камеры. Операция показана при закрытоугольной глаукоме в тех случаях, когда иридэктомия невозможна или неэффективна, а также при открытоугольной глаукоме с узким профилем угла передней камеры как предварительный этап для последующей трабекулопластики.
Лазерная пупиллопластика показана в тех случаях закрытоугольной глаукомы, когда иридэктомию не удается произвести. На зрачковую зону радужки в одном из ее секторов несколькими рядами наносят 20-30 коагулятов. Сокращение стромы радужки сопровождается подтягиванием зрачка в ту же сторону и освобождением угла передней камеры в противоположном.
Лечение глаукомы лазером, выполненное вовремя и по показаниям, является высокоэффективным методом хирургии глаукомы.
Лазерное лечение глаукомы эффективно более чем в 90% случаев при начальной стадии открытоугольной глаукомы, при развитой стадии глаукомы положительный результат лечения снижается до 83%, а при далеко зашедшей и терминальной стадиях составляет только 52% и 34% случаев соответственно. Снижение эффективности при первичной открытоугольной глаукоме по мере прогрессирования заболевания требует выполнения хирургического лечения, к тому же лазерная операция низкоэффективна при юношеской глаукоме и первичной глаукоме у лиц молодого возраста.
Методы лазерного лечения
Разработано около 10 общепринятых методик лазерной терапии глаукомы. Наибольшее распространение получили технологии циклокоагуляции, иридэктомии, трабекулопластики, непроникающей склерэктомии, осуществляющиеся с помощью лазера.
Циклокоагуляция
Лазерная циклокоагуляция позволяет добиться при глаукоме снижения внутриглазного давления даже в случае острых форм заболевания. Благодаря ей удается предупредить наступление осложнений: глаукомоциклических кризов, нейропатии зрительного нерва, увеитов.
Отростки ресничного тела участвуют в продуцировании внутриглазной жидкости. В ходе циклокоагуляции они прижигаются лазерным лучом. Это приводит к снижению выработки жидкости и снижению давления внутри глазного яблока.
Микроимпульсная циклокоагуляция снижает внутриглазное давление минимум на 80% от исходного и чаще применяется при острой глаукоме. Другая разновидность процедуры, транссклеральная диод-лазерная коагуляция, более предпочтительна при хронической. Оба метода рекомендуются с целью профилактики осложнений в позднем послеоперационном периоде.
Глубокая непроникающая склерэктомия
Это эффективная, но сложная методика, требующая высокой квалификации врача. Непроникающей она названа потому, что не затрагивается передняя камера глаза. Производится вскрытие Шлеммова канала без ножевого проникновения. Таким путем удается создать дополнительный путь оттока внутриглазной жидкости.
Иридэктомия
Лазерная иридэктомия чаще всего показана при закрытоугольной глаукоме. Во время операции лазер проделывает маленькое сквозное отверстие в радужной оболочке. Оно служит своеобразным дренажом. Это помогает нормализовать давление между камерами глаза.
Иридэктомия предотвращает приступы закрытоугольной глаукомы, переход острой формы болезни в хроническую. Также с ее помощью убираются спайки радужки.
Трабекулопластика
Лазерная трабекулопластика – самая частая неинвазивная процедура с лазером, использующаяся при глаукоме. В ее ходе происходит восстановление проходимости каналов трабекулярной сети глаза, через которую фильтруется внутриглазная жидкость.
Применяют две разновидности процедуры: аргоновая лазерная (АЛТ) и селективная (СЛТ). Более предпочтителен второй вид операции, т. к. в ее ходе используется низкотемпературный лазер. Процедуру СЛТ можно повторить от 4 до 6 раз, а АЛТ – не более 1.