Термин дистрофия с латыни переводится как «расстройство питания тканей». В основе дистрофических процессов любой локализации лежит нарушение метаболических процессов на клеточном уровне, которое приводит к появлению сначала структурных изменений, а затем и к функциональной недостаточности.
Дистрофия сетчатки – это сложная патология сетчатой оболочки глаза, которая приводит к стойкому ухудшению остроты зрения. Причиной ее появления является комплекс факторов, которые условно можно разделить на внешние (экзогенные) и внутренние (эндогенные). Непосредственной причиной появления дистрофии сетчатки являются сосудистые нарушения, запускающие каскад патологических реакций, в итоге приводящих к выраженному снижению зрения. Длительное время болезнь остается совершенно незаметной и обнаруживается зачастую уже при развитии осложнений.
В лечении большинства болезней глаз время их обнаружения имеет решающее значение, ведь чем раньше начато адекватное лечение, тем лучше прогноз с точки зрения сохранения зрения. Не лишайте себя возможности хорошо видеть, ежегодно проходите обследование глаз, даже если вам кажется, что симптомов болезней глаз у вас нет! Простая, быстрая и недорогая процедура осмотра глаз у офтальмолога поможет сберечь зрение на долгие годы!
Причины появления дистрофии сетчатки
Довольно часто дистрофии сетчатки генетически обусловлены, но есть ряд факторов, которые повышают вероятность развития болезни. К ним относятся:
- пожилой возраст
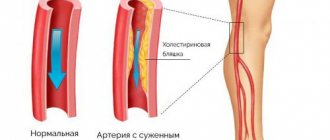
- болезни сердечно-сосудистой системы (гипертоническая болезнь, атеросклероз)
- сахарный диабет
- избыточный вес
- вредные привычки (курение, злоупотребление алкоголем, неправильное питание)
- близорукость средней и высокой степени
- тяжелые инфекционные заболевания, хронический стресс
- перенесенные воспаления глаз, травмы глазного яблока
Как проявляется дистрофия сетчатки
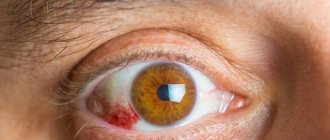
Общим симптомом для любой формы дистрофии является прогрессирующее ухудшение зрения, а также нарушение полей зрения. При осмотре глаз могут быть выявлены скотомы (участки выпадения зрения), искажение видимого изображения предметов, ухудшение ориентации в сумерках и в условии ограниченной освещенности. Больной с дистрофией сетчатки может заметить искривление прямых линий, непрозрачные пятна в поле зрения, выпадение букв во время чтения, изменение цветовосприятия.
На ранней стадии дистрофии сетчатки могут не вызывать никаких неприятных ощущений. Поэтому если вы или ваши родственники находитесь в группе риска, не игнорируйте ежегодный осмотр у квалифицированного офтальмолога.
Группы риска
Источник: setchatkaglaza.ru
Чаще всего дистрофия встречается у пожилых людей. К группе риска относятся люди, страдающие миопией, а также те, у кого имеются заболевания сосудов, диабет, гипертония.
Склонность к этому заболеванию наследуется, поэтому детям больных дистрофией сетчатки рекомендуется чаще проходит обследование глазного дна.
По статистике это заболевание чаще встречается у людей с белой коже и голубой радужкой глаза. Женщины болеют чаще мужчин.
Какие бывают дистрофии сетчатки
Дистрофия сетчатки – сборное понятие, которое объединяет разные по природе и проявлениям патологии сетчатой оболочки глаза. По своей природе дистрофии сетчатки разделяются на первичные, наследственно обусловленные, и вторичные, приобретенные, вызванные общими заболеваниями организма.
Первичные дистрофии сетчатки – это множество различных патологий, передающихся по наследству. Обычно они проявляются в детском возрасте и вызывают стойкое прогрессирующее снижение зрения, со временем приводящее к слепоте. Примером первичных дистрофий сетчатки являются амавроз Лебера, пигментная дистрофия сетчатки, болезнь Вагнера, дистрофия Беста, болезнь Штаргардта, точечно-белая дистрофия сетчатки.
Вторичные (приобретенные) дистрофии, в зависимости от преимущественной области поражения сетчатки, разделяют на центральные и периферические.
Чем грозит?
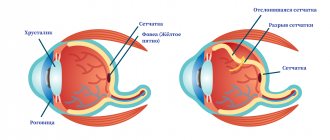
Прогноз напрямую зависит от вида дистрофии. При прогрессирующей миопии (близорукости), когда глаз удлиняется в течении всей жизни, развиваются дистрофические изменения на глазном дне – сетчатка перерастягивается и на ней образуются патологические очаги.
Они – возможный источник разрыва, поэтому пациенты со средней и высокой близорукостью находятся в группе риска по отслойке сетчатки.
Пигментная дистрофия сетчатки – хроническое медленно прогрессирующее состояние, поражающее молодых людей. При относительно хорошем центральном зрении, на далеко зашедших стадиях, сохраняется только небольшое “окно” здоровой сетчатки. Больной видит мир, как бы через узкую трубку.
Важно
Минус: к этой болезни наблюдается семейная предрасположенность. Плюс: возможна временная стабилизация и управление процессом при своевременном поддерживающем лечении не реже 2 раз в год.
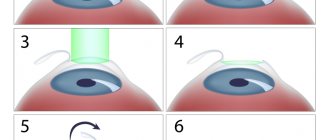
Желточная дистрофия Беста протекает в три стадии: формирование кисты, ее разрыв с кровоизлиянием и образование рубца на пораженном участке. Соответственно окончательные зрительные функции обусловливаются локализацией процесса.
Макулодистрофия Штаргардта и желто-пятнистая дистрофия Франческетти приводят к ощутимому снижению зрения, поскольку захватывают центральный отдел сетчатки – макулу.
Развитие вторичных дистрофий связано с прогрессированием основного заболевания – обычно на фоне хронической гипертонии, болезни почек или лейкоза развивается ангиопатия, которая способна перерастать в ретинопатию. Ее исход – дистрофия.
Говоря о дистрофии сетчатки у пожилых людей, нужно пояснить, что некоторые виды периферических изменений более опасны в плане возможной отслойки, чем остальные. К примеру, ретиношизис (расслоение) гораздо реже переходит в разрыв, чем та же решетчатая дистрофия.
Что касается возрастной макулодистрофии, то она безусловно снижает качество зрения пациента, но и в данном случае уровень дискомфорта зависит от формы – сухой или экссудативной. Первая, обычно, менее агрессивна, вторая – требует активного вмешательства и значительно влияет на функции глаза.
Центральные дистрофии сетчатки
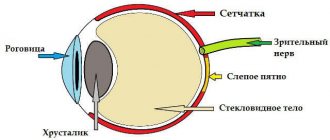
Поскольку при этой форме дистрофии сетчатки поражается область макулы (желтого пятна, центральной ямки сетчатки), заболевание также называют макулодистрофией. Желтое пятно, или макула – это область сетчатки, отвечающая за наилучшую остроту зрения и различие мелких деталей изображения. При поражении этой области страдает центральное зрение, а периферическое зрение остается неизменным. Человеку с центральной дистрофией сетчатки сложно читать, водить машину, рисовать, писать, вышивать и т.п.
В молодом возрасте центральная дистрофия сетчатки нередко выявляется при миопии, в пожилом возрасте диагностируют возрастную макулодистрофию. Своевременное выявление и регулярная терапия позволяют остановить прогрессирование симптомов заболевания и сохранить зрение на долгие годы.
Периферические дистрофии сетчатки
В этом случае изменения обнаруживаются на периферии сетчатки, то есть в тех ее областях, которые не принимают участия в формировании четкого зрения. Периферические ретинальные дистрофии, как правило, не сопровождаются отчетливым ухудшением зрения, но повышают риск развития тяжелых патологий глаз, таких как отслойка сетчатки.
Периферические дистрофии различной степени выраженности диагностируются у большинства близоруких людей. Поэтому если вы носите очки или линзы, обязательно проходите ежегодный осмотр глазного дна у офтальмолога. В случае, если доктор обнаружит участки истончения или разрывов сетчатки, вам будет предложена ограничительная лазерная коагуляция сетчатки.
Болезнь Беста и вителлиформная дистрофия взрослых
- Генетические исследования
- Гистологические и гистохимические исследования
- Классификация
- Клинические проявления
- Диагностика
- Дифференциальная диагностика
- Лечение
Болезнь Беста — редко встречающаяся двусторонняя макулодистрофия с разнообразными асимметричными клиническими проявлениями, наследуемая по аутосомно-доминантному типу. Заболевание впервые описано еще в 1883 г. J.E. Adams как «своеобразные» изменения в макуле.
В 1905 г. F. Best сообщил о 8 больных с макулярной дегенерацией из большой семьи, насчитывающей 59 человек, и предположил, что заболевание передается по аутосомно-доминантному типу.
Заболевание известно в литературе под следующими названиями:
- вителлиформная дистрофия Беста,
- центральная экссудативная отслойка сетчатки,
- наследственные макулярные псевдокисты,
- наследственная вителлиформная макулярная дегенерация
Наиболее характерным проявлением болезни Беста являются изменения в макуле, напоминающие яичный желток, диаметром от 0,3 до 3 РД.
Вителлиформная макулодистрофия взрослых впервые описана J.D.M. Gass в 1974 г. Заболевание развивается в возрасте 40-50 лет и характеризуется двусторонними симметричными локальными субретинальными изменениями в области фовеа. Очаги поражения обычно имеют округлую форму и желтый цвет, диаметр их варьирует от 0,3 до 0,5 РД. Зрительные нарушения минимальные.
В отличие от болезни Беста фовеолярные изменения при вителлиформной макулодистрофии взрослых развиваются в зрелом возрасте, имеют меньшие размеры и не прогрессируют.
Генетические исследования
Болезнь Беста — заболевание с аутосомно-доминантным типом наследования и высокой пенетрантностью. Ген, ответственный за развитие вителлиформной макулодистрофии, который называют «бестрофин», локализуется на длинном плече 11-й хромосомы в интервале между локусами D11S903 и PYGM (ген, кодирующий мышечную гликогенфосфорилазу) или, как показали более поздние исследования, между маркерами D11S986h D11S480.
Кроме того, в данной области был картирован ген ROM1, кодирующий фоторецепторспецифический мембранный белок. В связи с этим было высказано предположение, что болезнь Беста является результатом мутаций, возникающих в гене ROM1.
Н. Stohr и В.Н. Weber (1995), картировав ген ROM1, а также локусы D11S986, UGB (ген утероглобина) и PYGM, показали, что UGB локализуется проксимально по отношению к ROM1 и оба гена рекомбинируют при болезни Беста. Авторы сделали вывод, что ген ROM1 не имеет отношения к болезни Беста.
Перекрывающая приблизительно 40 сМ область 11q13-14, в которой локализуется ген «бестрофин», печально известна офтальмогенетикам как «прибежище» множества генов, ответственных за развитие ряда заболеваний сетчатки, в частности глазокожной формы альбинизма, синдрома Ушера («myosin 7A»), синдрома Барде-Бидля, аутосомно-доминантной формы семейной экссудативной витреоретинопатии.
R. E. Ferrell и соавт. (1983) при обследовании пациентов с атипичной семейной вителлиформной макулодистрофией выявили ее связь с классическим маркером GPT1, локализующимся на длинном плече 8-й хромосомы. У некоторых больных из обследованной ими семьи была нормальная ЭОГ, а диаметр очагов вителлиформных изменений в макуле во всех случаях не превышал 1 РД.
Высокая вариабельность клинических проявлений болезни Беста во многом объясняется генетической гетерогенностью и, помимо этого, может быть обусловлена неизвестными до настоящего времени мутациями. S. Nordstrom и W. Thorburn (1980) сообщили о семье, в которой у гомозиготного отца было 11 дочерей с различными клиническими проявлениями болезни Беста.
Вителлиформная макулодистрофия взрослых
Хотя в специальной литературе, посвященной вителлиформной дистрофии взрослых, не приводятся данные о семейных случаях, считается, что заболевание передается по аутосомно-доминантному типу. Недавно появились сообщения о том, что у пациентов с вителлиформной дистрофией взрослых обнаружена мутация Y258Stop в гене периферина/ЛАУ. При исследовании кодирующей области гена RDS из 28 больных с вителлиформной макулодистрофией взрослых у 18 % авторы определили пять новых мутаций, из которых две были нейтральными или полиморфизмами. Таким образом, нельзя исключить, что в ряде случаев изменения гена RDS также приводят к развитию вителлиформной дистрофии, однако механизм, посредством которого специфические мутации в этом гене могут вызывать дистрофии сетчатки, в том числе макулодистрофию, до сих пор не известен.
Гистологические и гистохимические исследования
В ходе исследований с использованием световой и электронной микроскопии установлено, что в ранних стадиях болезни Беста клетки пигментного эпителия поглощаются цитосомами с аномальной неидентифицируемой субстанцией. Между клетками пигментного эпителия сетчатки и нейроэпителия накапливаются гранулы липофусциноподобного вещества, нарушаются целостность мембраны Бруха и структура нервных элементов сетчатки: большая часть наружных сегментов фоторецепторов исчезает или дегенерирует, при этом во внутренних сегментах, фоторецепторов пораженных участков сетчатки происходит накопление кислых мукополисахаридов. Капилляры проникают в субретинальное пространство через измененную мембрану Бруха.
Во II стадии внутри клеток пигментного эпителия сетчатки в макуле происходит накопление значительного количества гранул вещества, гистохимически близкого липофусцину, а также макрофагов в субретинальном пространстве и в хороидее. В поздних стадиях заболевания отмечается уплощение клеток пигментного эпителия сетчатки в макуле, диаметр которых превышает норму в 1,5—2 раза.
У больных с вителлиформной дистрофией старшего и пожилого возраста диффузные отложения липофусциноподобного вещества были выявлены в слое пигментного эпителия, во внутренних сегментах фоторецепторов, внутри мюллеровских клеток и даже в стекловидном теле.
Классификация
В зависимости от офтальмоскопических проявлений выделяют пять стадий в течении болезни Беста:
- стадия О — изменении в макуле нет, но регистрируется аномальная ЭОГ
- стадия I — минимальные пигментные нарушения в макуле, гипопигментация;
- стадия II — классическая вителлиформная киста в макуле;
- стадия III — разрыв кисты и различные фазы резорбции ее содержимого;
- стадия IV — резорбция содержимого кисты, формирование фиброглиального рубца с субретинальной неоваскуляризацией или без нее.
В то же время нет убедительных доказательств того, что у большинства пациентов с болезнью Беста эволюция макулярных изменений проходит последовательно через все стадии.
Клинические проявления
Течение болезни Беста обычно бессимптомное, ее выявляют случайно при осмотре детей в возрасте 2-6 лет. Офтальмоскопические изменения в большинстве случаев асимметричны. В нулевой стадии глазное дно у детей обычно выглядит нормальным. Иногда отмечается ослабление фовеального рефлекса. Взрослых с подобной офтальмоскопической картиной расценивают как носителей патологического гена, что подтверждается снижением коэффициента Ардена — отношения светового пика к темновому спаду в ЭОГ.
- Для I, или «превителлиформной», стадии болезни Беста характерно появление мелких желтых пятнышек в макуле.
- Во II стадии болезни размеры вителлиформных кист, напоминающих «яичный желток», могут достигать диаметра диска. Изменения чаще двусторонние, но редко бывают симметричными. Острота зрения в этой стадии не соответствует офтальмоскопическим проявлениям, оставаясь даже у лиц пожилого возраста в пределах от 0,4 до 0,9.
- Снижение остроты зрения отмечается в III стадии заболевания, когда отдельные вителлиформные кисты разрываются, вызывая ассоциацию с «яичницей-болтушкой».
- Позднее в результате частичной резорбции и смещения липофусциноподобного содержимого кисты формируется картина псевдогипопиона.
В любой стадии заболевания у пациентов с болезнью Беста могут возникать субретинальные кровоизлияния. Приблизительно в 5 % случаев формируется субретинальная неоваскулярная мембрана.
S. A. Miller и соавт. (1976) сообщили о 9-летнем мальчике с болезнью Беста, у которого были обнаружены интактная вителлиформная киста правого глаза и вскрывшаяся, частично резорбировавшаяся киста с субретинальными геморрагиями и неоваскулярной мембраной слева.
А.Р. Schachat и соавт. (1985) наблюдали казуистический случай развития макулярного разрыва и регматогенной отслойки сетчатки у пациента с болезнью Беста. В преклонном возрасте у больных с данной патологией вследствие утраты хориокапилляров и атрофии пигментного эпителия сетчатки нередко развивается хороидальный склероз в макулярной области.
В литературе имеются сообщения о множественных вителлиформных поражениях при болезни Беста. В этих случаях макулярные вителлиформные изменения сочетаются с экстрафовеальными поражениями сетчатки, локализующимися, как правило, вдоль верхневисочной сосудистой аркады. Обычно насчитывается от 2 до 5 экстрамакулярных вителлиформных поражений. Их диаметр несколько меньше, чем размеры макулярных изменений, и не превышает 0,2-1 РД.
Поражения-сателлиты могут эволюционировать асинхронно по отношению друг к другу и к изменениям в макуле, а могут находиться на той же стадии развития.
Диагностика
Флюоресцентная ангиография
Ангиографическая картина при болезни Беста варьирует в зависимости от стадии заболевания. В начальной стадии болезни отмечается отсутствие флюоресценции в области кисты (так называемый блок флюоресценции). В превителлиформной стадии заболевания в зонах атрофии пигментного эпителия в макуле выявляют мелкие окончатые дефекты, обусловленные локальной гиперфлюоресценцией.
После разрыва кисты (стадия «псевдогипопиона») определяется гиперфлюоресценция в ее верхней половине, тогда как в нижней сохраняется «блок» флюоресценции. В поздней стадии заболевания, когда липофусциноподобное содержимое кисты частично резорбируется, в макуле выявляют окончатые дефекты.
Психофизические исследования
- Жалобы. Пациенты с болезнью Беста обычно предъявляют жалобы на затуманивание зрения, снижение остроты зрения, затруднения при чтении текстов с мелким шрифтом и метаморфопсии.
- Острота зрения. Острота зрения у пациентов с болезнью Беста варьирует в зависимости от стадии заболевания от 0,02 до 1,0. При длительном наблюдении за 58 пациентами с болезнью Беста в различных стадиях R. Clement (1991) установил, что у 43 % из них острота зрения составляла 0,5 и выше. G.A. Fishman и соавт. (1993), обследовав 47 пациентов с болезнью Беста II-IV стадий в возрасте 5-72 лет из 23 семей, обнаружили, что у 41 % из них острота зрения была не ниже 0,3. Между тем авторы отметили, что лишь у 20 % пациентов старше 40 лет зрение соответствовало требованиям водительской комиссии, а у всех пациентов старше 50 лет с офтальмоскопическими изменениями, соответствующими III-IV стадиям болезни, острота зрения лучше видящего глаза не превышала 0,1-0,3.
- Цветовое зрение. Цветовосприятие у большинства больных нормальное.
- Поле зрения. Периферические границы поля зрения сохраняются нормальными. При компьютерной статической периметрии у некоторых больных может быть выявлена относительная центральная скотома. Порог яркостной чувствительности в начальной стадии болезни у пациентов с высокой остротой зрения не изменяется.
- Электрофизиологические исследования. Общая и локальная ЭРГ при болезни Беста сохраняются нормальными. Единственным достоверным тестом, позволяющим диагностировать болезнь Беста, является электроокулография. Характерными признаками болезни Беста являются низкий базовый потенциал и снижение коэффициента Ардена — отношения светового пика к темновому спаду. Коэффициент Ардена у пациентов с болезнью Беста не превышает 1,5 (150 %). Изменения ЭОГ регистрируют не только у больных с клиническими проявлениями заболевания, но и у носителей патологического гена. У пациентов с вителлиформной макулодистрофией взрослых ЭОГ, как правило, не изменена.
Дифференциальная диагностика
Точный диагноз у пациентов с болезнью Беста и вителлиформной дистрофией взрослых устанавливают на основании офтальмоскопической картины и результатов регистрации ЭРГ и ЭОГ. В трудных случаях помощь в диагностике может оказать обследование других членов семьи.
Болезнь Беста необходимо дифференцировать от отслойки пигментного эпителия, болезни Коатса и острого токсоплазмозного хороиретинита.
- Отслойка пигментного эпителия. Сложности в диагностике возникают у пациентов с атипичной клинической картиной и экссудативными изменениями в макуле. Заболевание чаще одностороннее. Общая ЭРГ не изменяется, локальная ЭРГ может быть снижена. ЭОГ в большинстве случаев нормальная. При флюоресцентной ангиографии в поздней фазе у пациентов с отслойкой пигментного эпителия сетчатки выявляют гиперфлюоресценцию.
- Болезнь Коатса. У большинства больных с ретинитом Коатса во время первого обследования у офтальмолога в макуле выявляют проминирующий очаг твердого экссудата желтого цвета, напоминающий вителлиформные изменения при болезни Беста. Экссудативные изменения в макуле нередко сочетаются с субретинальными геморрагиями и неоваскуляризацией. Диагноз основывается на результатах офтальмоскопии: при осмотре периферии глазного дна с использованием налобного офтальмоскопа и линз 20-30 дптр или биомикроскопии с трехзеркальной линзой Гольдманна у всех пациентов с болезнью Коатса выявляют сосудистые аномалии (телеангиэктазии, микро- и макроаневризмы, артериовенозные шунты), чаще локализующиеся в височной половине сетчатки. Заболевание спорадическое. У 92-95 % больных поражается один глаз. ЭОГ в начальной и развитой (ПА) стадиях болезни не изменяется. Острота зрения у пациентов с ретинитом Коатса при наличии экссудативных изменений в макуле не превышает 0,4.
- Острый токсоплазмозный хороиретинит. Диагностические трудности возникают обычно при обследовании пациентов с приобретенной формой токсоплазмоза и экссудативно-геморрагическими изменениями в макуле. Заболевание, как правило, одностороннее. Хороиретинальные поражения сочетаются с витреитом различной тяжести, а иногда и с изменениями переднего отрезка. Такие пациенты обычно жалуются на внезапное значительное снижение остроты зрения, которая в большинстве случаев варьирует от 0,01 до 0,2. При статической периметрии выявляют повышение порога яркостнои чувствительности и абсолютную или относительную центральную скотому. Подтвердить диагноз токсоплазмоза позволяют положительные результаты иммунологических исследований.
Лечение
Для пациентов с болезнью Беста и вителлиформной макулодистрофией взрослых не существует эффективного лечения, и с целью исключения любых возможных осложнений, таких как ХНВ, сквозные макулярные отверстия или отслоение сетчатки, необходимо проводить комплексное обследование глаз пациентов, включая дилатацию, один или два раза в год. При нарушении зрения пациентов следует направлять на исследование снижения зрения и медицинскую реабилитацию.
На короткое время могут быть эффективны инъекции ранибизумаба в стекловидное тело. Прогноз по зрению достаточно благоприятен, потому что болезнь обычно приводит к медленно прогрессирующей потере зрения, и большинство пациентов поддерживает неплохое зрение хотя бы одного глаза до последних стадий болезни. Вителиформная дегенерация обычно исчезает в течение жизни, однако на поздних атрофических стадиях болезни может наблюдаться потеря зрения, образование сквозных макулярных отверстий или отслоение сетчатки.
Поддерживающая терапия:
- Милдронат 5,0 в/в №10, затем по 1 капсуле 2 раза в день, 1 месяц
- Мексидол 2,0 в/м №10, затем по 1 таб. 3 раза в день, 1 месяц
- Эмоксипин 1% по 1 капле 3 раза в день, 1 месяц
- Мильгамма 2,0 №5 в/м ч/д
- Нутроф форте по 1 таблетке 1 раз в день постоянно
Лечение дистрофии сетчатки
Своевременно начатое лечение дистрофии сетчатки помогает улучшить остроту зрения, остановить прогрессирование патологических изменений в тканях глаза и предотвратить появление грозных осложнений.
Для лечения дистрофий сетчатки применяют комплексный подход. Ввиду того, что большинство случаев заболевания носит наследственный характер, лечение болезни их симптоматическое, направленное на поддержание достаточной остроты зрения.
Медикаментозное лечение включает применение лекарственных препаратов с различным механизмом действия, цель которого – улучшение питания тканей сетчатки. Обычно применяют сосудорасширяющие препараты (но-шпа, папаверин), дезагреганты (аспирин, клопидогрель), комплексные витаминные препараты, укрепляющие стенки сосудов сетчатки (аскорутин, препараты с лютеином), биогенные стимуляторы и пептиды (ретиналамин, экстракт алоэ). При обнаружении экссудативной формы ВМД показаны интравитреальные инъекции препаратов из группы блокаторов неоангиогенеза (anti-VEGF препараты), дексаметазона, рассасывающих препаратов (гепарин, этамзилат).
Физиотерапевтическое лечение при дистрофии сетчатки включает магнитотерапию, лазерную стимуляцию сетчатки, электрофорез с лекарственными препаратами, улучшающими питание тканей (но-шпа, никотиновая кислота и пр.).
Аппаратное лечение возможно и в домашних условиях — использование прибора АМВО-01, разработанного специально для применения у пациентов с патологией сетчатки и зрительного нерва.
Наиболее эффективным методом лечения у пациентов с дистрофиями сетчатки является лазерная коагуляция (фотокоагуляция) сетчатки. Цель такого лечения – отграничение измененных областей сетчатки от окружающих их здоровых тканей для предотвращения прогрессирования болезни и развития возможных осложнений. Местное воздействие лазерных лучей повышает температуру в области обработки и вызывает ограниченную коагуляцию тканей и образование прочных сращений между сетчаткой и прилежащей к ней сосудистой оболочкой.
Хирургическое лечение показано при выявлении грубых сращений (шварт) между сетчаткой и стекловидным телом глаза, а также неоваскулярных мембран. С этой целью применяют витреоретинальные операции (витрэктомия, склеропломбаж, экстрасклеральное пломбирование и пр.).
Методы диагностики
Источник: visus-1.ru
Помимо базового обследования при заболеваниях сетчатки для постановки правильного диагноза необходимо провести следующие исследования:
- Оптическая когерентная томография сетчатки – бесконтактное, высокоточное исследование сетчатки на уровне структуры тканей.
Метод позволяет получить исчерпывающее представление об ультраструктуре любого участка сетчатки.
Все измерения проводятся в микронах и очень точно отражают малейшие изменения. Оптическая когерентная томография – это один из наиболее точных и универсальных методов исследования в офтальмологии, абсолютно необходимый при заболеваниях сетчатки.
RTVue-100 позволяет значительно расширить возможности исследования и повысить точность диагностики, и является абсолютно необходимым в диагностике и при лечении заболеваний сетчатки.
В современной офтальмологии именно результаты этого исследования являются решающими в выборе тактики лечения и контроле за его эффективностью.
- Квантитативная статическая периметрия – очень точный метод исследования поля зрения
Позволяет выявить малейшие функциональные дефекты поля зрения и получить их количественную оценку. Контрольные исследования в течение года позволяют объективно оценить изменения размеров и формы патологического очага.
Сравнение полученных в течение времени изображений даёт возможность оценить динамику заболевания и эффективность проводимого лечения.
- Фоторегистрация глазного дна и фаг (флюоресцентная ангиография)
Достаточно часто во время обследования у врача возникает необходимость не только детально рассмотреть картину глазного дна (сетчатку, сосуды глаза, диск зрительного нерва), но и получить увеличенное изображение определённых деталей, а также зафиксировать имеющиеся изменения.
Особенно это важно в тех случаях, когда предполагается дальнейшее наблюдение за процессом с целью оценки эффективности лечения и наблюдения за его динамикой. В этих случаях врач прибегает к специальному фотографированию глазного дна.
Осуществляется такое фотографирование с помощью цифровой фундус-камеры. Полученные изображения сохраняются в архиве, изображение также копируется на СD-диске и выдаётся пациенту.
- Флюоресцентная ангиография глаза (ФАГ) – объективный метод исследования сосудов глаза при их контрастировании флюоресцеином.
Метод незаменим для уточнения диагноза при заболеваниях сетчатки. Без этого исследования невозможно принять обоснованного решения о тактике лечения конкретного пациента с заболеванием сетчатки.
ФАГ необходим при следующих заболеваниях:
- возрастная макулярная дегенерация,
- диабетическая ретинопатия и диабетический макулярный отёк,
- тромбоз вены сетчатки,
- центральная серозная хориоретинопатия,
- воспалительные процессы в сетчатке и зрительном нерве.
Диагностика заболевания включает исследование глазного дна, определение остроты зрения, оценку зрительных полей и оценку цветовосприятия. Исследовать глазное дно при подозрениях на периферическую дистрофию сложнее.
Необходимо медикаментозно расширять зрачок и изучать глазное дно с помощью трехзеркальной линзы Гольдмана.
С помощью оптической когерентной томографии врач может получить трехмерный снимок ретины глаза. Жизнеспособность клеток сетчатки и нервных окончаний изучают с помощью электрофизиологического исследования. Иногда используют УЗИ.
Для того, чтобы подтвердить или опровергнуть диагноз «дистрофия сетчатки», необходимо пройти тщательное обследование зрительной системы.
Обследование пациентов с подозрением на дистрофию сетчатки включает в себя:
- определение остроты зрения;
- исследование полей зрения (периметрия) для того, чтобы оценить состояние сетчатки на ее периферии;
- оптическая когерентная томография;
- электрофизиологическое исследование – определение жизнеспособности нервных клеток сетчатки и зрительного нерва;
- ультразвуковое исследование внутренних структур глаза – А-сканирование, В-сканирование;
- измерение внутриглазного давления (тонометрия);
- исследование глазного дна (офтальмоскопия).
Прочие инструментальные методы:
- визометрия – субъективное определение остроты зрения, первичный подбор коррекции (очков);
- периметрия – анализ полей зрения, поиск тех самых “слепых” пятен;
- оптическая когерентная томография – современный метод бесконтактной диагностики, который заключается в пошаговой съемке сетчатки.