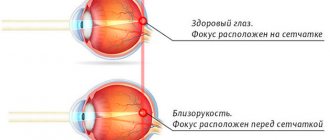
«Золотым стандартом» лечения некоторых заболеваний заднего отрезка глаза является anti-VEGF терапия, а именно процедура интравитреального введения препаратов «Эйлеа» (Eylea) или «Луцентис» (Lucentis).
VEGF
(англ. vascular endothelial growth factor) — фактор роста эндотелия сосудов.
Аnti-VEGF
— антитела к фактору роста эндотелия сосудов.
Цель anti-VEGF терапии — уменьшить патологическую неоваскуляризацию (разрастания сосудов) и избыточную проницаемость новообразованных сосудов.
Эта цель достигается путем блокирования факторов роста эндотелия новообразованных сосудов, которые из-за своего некорректного строения приводят к возникновению рецидивирующих кровоизлияний и обширных отеков сетчаткиСетчатка
— внутренняя оболочка глаза, важная часть зрительного анализатора. Именно она отвечает за процесс превращения света в нервный импульс, который передается в головной мозг.. Такой аномальный рост возникает из-за воздействия различных факторов, приводящих к необходимости улучшения кровоснабжения пораженной ткани сетчатки
Сетчатка
— внутренняя оболочка глаза, важная часть зрительного анализатора. Именно она отвечает за процесс превращения света в нервный импульс, который передается в головной мозг. путем образования новых сосудов.
Данные результатов клинических исследований использования анти-VEGF препаратов
Системное применение в качестве внутривенных вливай. Имеются данные результатов только одного исследования внутривенного применения бевацизумаба, связанного с офтальмологической патологией. Это лечение 18 пациентов страдающих неоваскулярной ВМД. В данном неконтролируемом исследовании применявшаяся доза препарата составляла 5 мг/кг в 1, 2 и 3 инъекциях, которые выполнялись с интервалом в 2 недели. Острота зрения пациентов в ходе исследования повышалась уже спустя две недели от начала введения препарата и сохранялась на достигнутом уровне в течение 24 недель наблюдения. К концу исследования было выявлено значимое уменьшение толщины сетчатки. При этом, только шести лечившимся пациентам, за период наблюдения проводилась дополнительная терапия. Несмотря на полученные впечатляющие результаты исследования, его не планировали с целью выявления возможного побочного действия.
Интравитреальное введение. Достаточно масштабные клинические исследования были проведены на предмет применения пегаптаниба и ранибизумаба у пациентов с ВМД. Было выявлено, что пегаптаниб обладает меньшей эффективностью, чем ранибизумаб. Однако, применение его связано с меньшими рисками возникновения нежелательных последствий. Так по результатам трех центральных исследований с применением ранибизумаба получены данные об увеличении частоты случаев сердечно-сосудистых нарушений, в том числе инсультов и кровотечений, хотя данное повышение статистически не было значимым.
В нескольких проведенных исследованиях сообщается о выявлении положительных результатах лечения больных с сахарным диабетом. В двойном слепом проспективном контролируемом многоцентровом дозозависимом исследовании, которое охватило 172 пациента, страдающих диабетическим макулярным отеком, участники получали пегаптаниб и к концу исследования (через 36 недель) имели лучший прогноз по функции зрения. Было установлено уменьшение толщины центральной сетчатки и меньше случаев потребовали проведения дополнительного лазерного лечения.
В настоящий момент бевацизумаб применяется многими офтальмологами мира в качестве предоперационной терапии пролиферативной ДР перед витрэктомией.
Анти-VEGF терапия
- VEGF
- VEGF-опосредованная патология
- Ингибиторы VEGF
- Ранибизумаб (Луцентис, Lucentis)
- Бевацизумаб (Авастин, Avastin)
- Бролуцизумаб (Беову, Beovu)
- Пегаптаниб (Макуген, Макуджен)
- Афлиберцепт (Айлия, Эйлеа, Eylea)
Данный метод лечения основан на локальном ингибировании фактора роста эндотелия сосудов (VEGF: vascular endothelium growth factor) при обнаружении неоваскуляризации сетчатки (например при диабетической ретинопатии (ДМО), влажной форме ВМД, а также при посттромботической неоваскуляризации), тем самым останавливается рост новых хрупких сосудов с повышенной проницаемостью стенки. Иингибиторы VEGF могут быть альтернативой или дополнением к традиционному лазерному лечению и применению триамцинолона у больных с ДМО.
Разработка и внедрение в практику ингибиторов VEGF для интравитреального введения открыли новые перспективы в лечении ДМО. Использование анти-VEGF терапии, как в качестве единственного метода лечения, так и в сочетании с ЛКС, уменьшает выраженность отека макулы и повышает остроту зрения. В настоящее время для лечения ДМО в России зарегистрирован ранибизумаб (Луцентис, Genentech/Novartis). Показанием к назначению данного препарата является макулярный отек со снижением зрения и толщиной сетчатки в макулярной зоне более 300 мкм. Вместе с тем, положительные результаты в рандомизированных клинических исследованиях получены при применении бевацизумаба, пегаптаниба и афлиберцепта. В проводимых в настоящее время исследованиях планируется сравнить эффективность данных препаратов в лечении ДМО (NCT01610557, NCT01627249).
Анти-VEGF препараты вводятся интравитреально, так как это наиболее эффективный способ доставки лекарства непосредственно к сетчатке. При ИВВ в стекловидном теле остается до 51,4%, в сетчатку и сосудистую оболочку проникает до 13,2% введенной дозы. При других способах введения — суюконъюнктивальном и субтеноновом — в стекловидное тело, сетчатку и сосудистую оболочку проникает не более 5,3% введенной дозы.
VEGF
Впервые VEGF был выделен в 1983 году, как фактор способствующий увеличению сосудистой проницаемости в опухолях. VEGF относится к семейству гомодимерных гликопротеинов, сходный по структуре с фактором роста тромбоцитов, и связывается с пятью типами рецепторов с тирозин-киназной активностью. Множество физиологических и патологических процессов, связанных с нарушениями в системе VEGF-VEGFR, включают эмбриогенез, регулирование репродуктивной функции у женщин, беременность, заживление ран, рост опухолей, развитие ДР и ишемических болезней.
VEGF — мощный мультифункциональный цитокин, необходимый для процессов эмбриогенеза и раннего постнатального ангиогенеза. У взрослых VEGF в сосудистой стенке действует на разных уровнях: как фактор, обеспечивающий выживание эндотелиальных клеток, усиливает сосудистую проницаемость и действует как мощный вазодилятатор, участвует в регенерации мышечных клеток, ремоделировании миокарда и эндохондральном костеобразовании, он действует как хемоаттрактант, мобилизующий эндотелиальные клетки костного мозга. Помимо физиологического действия VEGF имеет и другие эффекты, которые, хотя и запускаются определенными патогенетическими механизмами, являются полезными. Они включают в себя способность индуцировать образование коллатерального кровообращения, которое необходимо для выживания клеток под действием гипоксии, и улучшение трофики в процессе заживления ран.
Семейство VEGF у человека включает факторы VEGF-A, -B, -C, -D, а также плацентарный фактор роста (PlGF). В настоящее время наиболее изучен VEGF-A, экспрессируемый во многих стромальных и паренхиматозных клетках и циркулирующий в кровотоке. У больных СД (сахарный диабет) с различной выраженностью ангиопатий зафиксировано повышение уровня VEGF-А в плазме крови и в моче. Вследствие гематоретинального барьера содержание VEGF в сетчатке зависит главным образом от локального образования фактора. Продуцентами VEGF в сетчатке являются клетки пигментного эпителия, астроциты, клетки Мюллера, эндотелиоциты, перициты и ганглионарные клетки. Действуя ауто- и паракринным путем, VEGF избирательно стимулирует пролиферацию и миграцию эндотелиальных клеток и их предшественников, увеличивает сосудистую проницаемость, способствует вазодилатации через усиление продукции оксида азота (NO).
В последние годы показано, что VEGF обеспечивает выживание и структурную целостность ретинального пигментного эпителия, оказывает антинейродегенеративный эффект и препятствует апоптозу ретинальных клеток в условиях ишемии-реперфузии.
Молекулярные изоформы VEGF (VEGF121, VEGF145,VEGF165, VEGF189, VEGF206) являются продуктами одного гена, образующимися в результате альтернативного сплайсинга мРНК. В гене VEGF выявлены полиморфные позиции -634, +936, -2578; обнаружены взаимосвязи вариантов нуклеотидов в этих позициях с риском развития диабетической ретинопатии (ДР) в разных этнических группах.
В настоящее время гиперпродукции VEGF отводят ведущую роль в повышении проницаемости ретинальных сосудов, развитии отека макулы и неоваскуляризации сетчатки при СД. Мощным триггером повышения синтеза VEGF и его рецепторов при ДР является гипоксия или ишемия сетчатки. Кроме того, продукцию VEGF в ретинальных клетках запускают гипергликемия и связанные с ней биохимические аномалии: накопление поздних продуктов гликирования, стресс эндоплазматического ретикулума, окислительный стресс.
VEGF-опосредованная патология
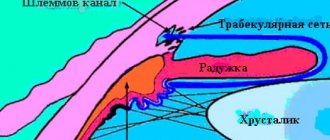
Сетчатка является наиболее активно метаболирующей тканью человека-интенсивность обмена веществ и энергопотребления в пересчете на единицу массы ткани намного превышает таковую во всех остальных тканях организма. Сложные биохимические процессы, сопровождающие трансформацию энергии кванта света при его поглощении фоторецепторами в энергию биоэлектрического импульса и последующую трансдукцию этого потенциала по биполярным и ганглиозным клеткам, требуют постоянного обеспечения ретинальной ткани адекватной трофикой.
Для этой цели в глазу человека одновременно существуют две коллекторные сосудистые системы: сосудистая оболочка (хориоидея), кровоснабжающая наружные отделы сетчатки, включая фоторецепторы, и собственные сосуды сетчатки, отвечающие за кровоснабжение внутренних слоев сетчатки, в том числе биполярных и ганглиозных клеток. Специфической анатомической особенностью сосудов сетчатки является то, что они не имеют коллатералей. Состоятельность и нормальное функционирование обеих сосудистых систем является основой нормальной жизнедеятельности ретинальной ткани.
В случаях нарушения кровоснабжения по любому из сосудистых коллекторов (независимо от этиологии и динамики развития) в сетчатке возникает состояние ишемии, что неизбежно сопровождается той или иной степени утратой функциональной активности сетчатки с последующим развитием дистрофических и атрофических изменений. Недостаток кислорода запускает в ишемизированной сетчатке каскад патологических процессов, многие этапы которых опосредованы специфическим белковым субстратом- эндотелиальным сосудистым фактором роста.
VEGF продуцируется эндотелиоцитами, перицитами, клетками пигментного эпителия сетчатки, присутствует в сетчатке в норме и регулирует ее гомеостаз. В случаях возникновения ишемии продукция VEGF в сетчатке возрастает в значительной степени, что является попыткой организма справиться с ишемией за счет расширения существующих сосудов или роста новых. При этом превышаются компенсаторные возможности физиологических механизмов регуляции содержания VEGE. B результате дисрегуляции контроля содержания сосудистого эндотелиального фактора роста происходит его избыточная секреция, что приводит к таким функциональным и анатомическим нарушениям собственных нормальных сосудов глазного яблока, как:
- фенестрирование эндотелия сосудов
- повышение проницаемости сосудов
- нарушения формы и морфологической структуры сосудов и др.
На макроуровне подобные изменения сопровождаются нарушением функции сосудов хориоидеи или сетчатки с развитием транссудации и экссудации (отека), кровоизлияний. В достаточно короткие сроки развивается следующий этап патологического процесса — появление новообразованных сосудов или интраокулярная неоваскуляризация, которая может развиваться в различных структурах глаза. Ключевая роль в индукции неоангиогенеза принадлежит избыточной концентрации VEGF в ретинальной ткани.
В зависимости от источника ишемии (хориоидея или собственные сосуды сетчатки) можно выделить два типа интраокулярной неоваскуляризации: хориоидальную и ретинальную. Они характеризуются различной морфологической и клинической картиной, имеют специфические особенности развития и прогрессирования. Общим для всех типов интраокулярной неоваскуляризации является неполноценность новообразованных сосудов, заключающаяся в отсутствии эндотелиальной базальной мембраны, вследствие чего в сосудистой стенке имеются множественные фенестры, приводящие к транссудации, экссудации и геморрагии. Подобные изменения характерны и для любого раневого или воспалительного процесса, когда имеет место нарушение целостности ткани.
Вслед за повреждением (альтерацией) следует экссудативная реакция, а далее начинается этап рубцевания алгоритм в организме, направленный на восстановление целостности структуры ткани путем интенсивной пролиферации соединительной ткани и сопровождающийся частичной или полной утратой специфической тканевой функции. Рубцевание как на поверхности сетчатки, под ней, так и в самой сетчатке неизбежно сопровождается утратой функции зрения. Тем самым предназначенный для устранения ишемии компенсаторный механизм интраокулярной неоваскуляризации становится губительным с точки зрения функциональной состоятельности органа, еще один универсальный алгоритм в организме, направленный на восстановление целостности структуры ткани путем интенсивной пролиферации соединительной ткани и сопровождающийся частичной или полной утратой специфической тканевой функции. Рубцевание как на поверхности сетчатки, под ней, так и в самой сетчатке неизбежно сопровождается потерей зрительных функций.
VEGF является не единственным участником сложных и разноплановых процессов, протекающих в сетчатке при различных ишемических состояниях, однако сегодня это наиболее изученное звено патогенеза, для которого определены не только роль и место, но и разработаны методы лечебного воздействия и регулирования, позволяющие эффективно влиять на патологический процесс и контролировать заболевание. Хотя нозологические формы, в патогенезе которых принимает участие VEGF, существенно различаются, наличие общего принципиального патогенетического звена в виде VEGF позволяет объединить все эти заболевания термином «VEGF-опосредованная патология».
Ингибиторы VEGF
| Ингибиторы VEGF | ||||
| Препарат | Торговое название | Разработчик | Характеристика | Специфичность связывания |
| Ранибизумаб | Lucentis | Genentech | Фрагмент рекомбинантных гуманизированных антител к VEGF-A | Связывает все изоформы VEGF-A |
| Бевацизумаб | Avastin | Genentech | Рекомбинантные гуманизированные антитела к VEGF-A | Связывает все изоформы VEGF-A |
| Бролуцизумаб | Beovu | Novartis | Гуманизированный одноцепочечный фрагмент антитела | Связывает все изоформы VEGF-A |
| Пегаптаниб | Macugen Eyetech | Pharmaceutical/ Pfizer | Пегилированный аптамер РНК | Связывает VEGF165 |
| Афлиберцепт | Eylea VEGF Trap-Eye Regeneron | Pharmaceutical/ Sanofi-Aventis | Рекомбинантный белок, напоминающий антитело, получен путем слияния надмембранной части рецептора VEGF (в качестве антиген-связывающего фрагмента, Fab) и IgG (в качестве Fc- фрагмента) | Связывает VEGF-A, VEGF-B и PlGF |
| Бевасираниб | — | OPKO | Малая интерферирующая РНК | Ингибирует транскрипцию генов VEGF |
Различия между ингибиторами VEGF касаются технологии получения, структуры и специфичности в отношении различных изоформ регулятора. Механизм действия анти-VEGF препаратов реализуется через непосредственное связывание с фактором роста (ранибизумаб, бевацизумаб, пегаптаниб), ингибирование экспрессии гена VEGF (бевасираниб) или его рецептора (афлиберцепт). В настоящее время клинические исследования II–III фазы при ДМО прошли ранибизумаб, бевацизумаб, пегаптаниб и афлиберцепт.
Ранибизумаб (Луцентис, Lucentis)
Данный ингибитор VEGF был специально разработан для применения в офтальмологии. В 2006 г. препарат разрешен Food and Drug Administration (FDA) для лечения неоваскулярной (влажной) возрастной дегенерации макулы. В настоящее время является единственным анти-VEGF препаратом, зарегистрированным для лечения ДМО в России. Эффективность ранибизумаба в лечении макулярного отека доказана в серии рандомизированных многоцентровых исследований, выполненных по стандартам GCP.
Бевацизумаб (Авастин, Avastin)
Данный препарат зарегистрирован для применения при метастатическом колоректальном раке, раке молочной железы и некоторых других злокачественных опухолях, в офтальмологии применяется «off-label». Изучению бевацизумаба в лечении ДМО посвящено более 40 исследований [ClinicalTrial.gov].
В настоящее время проводятся новые исследования, сравнивающие эффекты бевацизумаба и глюкокортикоидов: триамцинолона, дексаметазона (NCT01572350, NCT01571232, NCT01787669), бевацизумаба и ранибизумаба (NCT01635790, NCT01627249) в лечении ДМО.
Бролуцизумаб (Беову, Beovu)
Молекула бролуцизумаба (RTH258) – это гуманизированный одноцепочечный фрагмент антитела, способный связывать все изоформы VEGF-A. Бролуцизумаб обладает наименьшим молекулярным весом, составляющим 26 кДа, по сравнению с 115 кДа у афлиберцепта и 48 кДа у ранибизумаба (Gaudreault J. et al., Tietz J. et al.). Благодаря низкому молекулярному весу концентрация бролуцизумаба при его разведении может быть увеличена до 120 мг/мл, то есть при одной интравитреальной инъекции становится возможным ввести 6 мг бролуцизумаба в 0,05 мл раствора. По молекулярной массе 6 мг бролуцизумаба соответствуют примерно 12 дозам афлиберцепта 2 мг и 22 дозам ранибизумаба 0,5 мг (Tietz J. et al.). Интравитреальное введение препарата в большей концентрации потенциально может сопровождаться большей продолжительностью его действия.
Пегаптаниб (Макуген, Макуджен)
В США и в странах Европы селективный ингибитор VEGF165 пегаптаниб разрешен для лечения неоваскулярной формы возрастной макулярной дегенерации. В нескольких исследованиях оценивали эффект препарата при ДМО. Анализ ретроспективных данных показал способность пегаптаниба при введении в дозе 0,3 мг улучшать остроту зрения в первые 6 недель после инъекции. Для получения значимого эффекта в течение 6 месяцев требовалось выполнить не менее трех инъекций.
Афлиберцепт (Айлия, Эйлеа, Eylea)
Препарат обладает наиболее широким спектром анти-VEGF активности, связывает VEGF-A, VEGF-B и PlGF. В США одобрен для лечения влажной возрастной дегенерации макулы и метастатического колоректального рака. Исследования афлиберцепта (VEGF Trap-Eye) при ДМО начались позднее, чем других анти-VEGF препаратов.
Из новейших препаратов, подавляющих экспрессию VEGF, которые в настоящее время исследуются для лечения МО, можно назвать бевасираниб (OPKO Health, США). Это препарат на основе РНК, который также вводится интравитреально и подавляет ген, продуцирующий VEGF.
«VEGF Trap-Eye» (Regeneron, США и Bayer HealthCare, Германия) — препарат, который изначально разрабатывался в качестве противоопухолевого средства, является «ловушкой» для VEGF, так как его молекула имеет сходную структуру с рецептором VEGF. Препарат вводится интравитреально и блокирует все изоформы VEGF-A, а также PlGF12.
Офтальмологические осложнения при применении анти-VEGF терапии включают эндофтальмит, повышение внутриглазного давления, повреждение хрусталика и отслойку сетчатки. Частота этих осложнений, по данным большинства исследований, не превышает 1–1,5 случая на пациента в год. Системные побочные реакции также наблюдаются редко и включают повышение артериального давления, инсульт, инфаркт миокарда, протеинурию. Данные реакции могут быть связаны с проникновением небольшого количества препарата в кровоток. Получены данные, что уровень VEGF в кровотоке остается сниженным в течение месяца после интравитреального введения бевацизумаба и не снижается после введения ранибизумаба и пегаптаниба. В настоящее время инициировано исследование, призванное оценить степень «утечки» ингибиторов VEGF в циркуляцию при интравитреальном введении (NCT01661946). Требуется специально оценить безопасность ингибиторов VEGF у «проблемных» категорий больных СД с макрососудистыми осложнениями, тяжелой артериальной гипертензией и нефропатией. В будущих исследованиях предстоит определить оптимальную длительность анти-VEGF терапии, предикторы ее эффективности и целесообразность сочетания с другими методами лечения ДМО.
Применение гипотензивных препаратов (1 капля на ночь 14 дней) с целью профилактики повышения ВГД как в раннем, так и в позднем послеоперационном периоде позволяет предупредить возникновение офтальмогипертензии, а также улучшить микроциркуляцию в зоне поражения.
Нежелательные эффекты от введения ингибиторов VEGF
Анти-VEGF препараты вводят внутрь стекловидного тела непосредственно через прокол склеры, однако их проникновение в системный кровоток все же возможно. В свою очередь, это может привести к возникновению нежелательных системных проявлений. При этом, как маркеры системного влияния анти-VEGF препаратов, могут рассматриваться гипертензия и протеинурия, которые выявляются особенно часто при применении последних в лечении онкологических заболеваний. Повышение артериального давления становится следствием повышения уровня периферического сосудистого сопротивления из-за подавления выработки эндотелиальными клетками оксида азота, образование которого стимулирует VEGF посредством активации NO-синтазы, но также объяснимо изменением почечной функции. Прочие потенциальные осложнения, которые наблюдались в результате применения анти-VEGF, включают подавление процессов регенерации мышечной ткани с ремоделированием миокарда, бесплодие, изменение процесса заживления ран с формированием коллатерального кровообращения, кровотечения в ЖКТ.
Таким образом, потенциально возможные системные эффекты применения ингибиторов VEGF (включая, гипертензию, протеинурию, нарушения заживления раневых поверхностей, коллатерального кровообращения и пр.) могут быть опасны, особенно у лиц с сахарным диабетом.
Среди офтальмологических проявлений анти-VEGF препаратов, стоит отметить эндофтальмит, повреждения хрусталика и отслойку сетчатки, как наиболее часто отмечавшиеся. Серьезные осложнения, возникающие в ответ на интраокулярные введения препаратов, встречаются довольно редко. При этом, кумулятивный риск намного выше у лиц с сахарным диабетом, которые много лет требуют повторного лечения.
Помимо побочных эффектов от самой интравитреальной инъекции, возникают иные потенциальные нежелательные эффекты, развитие которых обусловлено подавлением действия VEGF. Необходимо отметить, что образованный пигментными ретинальными клетками VEGF обеспечивает функции хориокапилляров и обладает нейропротективным действием при ишемии сетчатки. Интересно, что когда для подавления VEGF применяли пегаптаниб, который не способен связываться с VEGF120 (или VEGF121 человека), уменьшения числа ганглиозных ретинальных клеток не выявлялось.
Очень часто, при интравитреальном введении бевацизумаба (блокирующего любые известные формы VEGF) никакого токсического действия на ганглиозные ретинальные клетки не наблюдается. Однако стоит отметить, что до настоящего момента не получено доказательств его повреждающего воздействия на сетчатку, которое можно было бы выявить при световой микроскопии. И тем не менее митохондриальные разрушения внутренних сегментов фоторецепторов (выявленное в результате электронной микроскопии), а также усиление апоптоза было отмечено в эксперименте на глазах крыс после интравитреального введения препарата.
На сегодняшний день, разработки ингибиторов VEGF, подавляющих патологические эффекты VEGF с одновременным сохранением нейропротективного действия, продолжаются, и это наверняка станет значимым прорывом при обеспечении безопасности новых лекарственных средств.
Ингибиторы VEGF
Ингибиторы VEGF различаются некоторыми аспектами, связанными с их получением, а также деталями структуры веществ и специфичности по отношению к различным изоформам регулятора. Действие препаратов анти-VEGF (ранибизумаб, бевацизумаб, пегаптаниб) обусловлено непосредственным связыванием с фактором роста, подавлением экспрессии гена VEGF либо его рецептора. К настоящему моменту II–III фазы клинических исследований терапии ВМД прошли: бевацизумаб, пегаптаниб, ранибизумаб, афлиберцепт. Большинство из них, уже официально одобрены в качестве средств лечения возрастной дегенерации макулы.
Ранибизумаб (Луцентис, Lucentis)
Вещество, содержащееся в препарате Луцентис, было специально адресовано офтальмологам. Данный ингибитор VEGF был разрешен Food and Drug Administration (FDA) для применения в США при лечении возрастной влажной дегенерации макулы. Сегодня, это единственный препарат с анти-VEGF действием, официально зарегистрированный в России. Его эффективность в лечении отека макулы доказана серией рандомизированных исследований, проведенных с охватом многих офтальмологических центров.
Бевацизумаб (Авастин, Avastin)
Этот анти-VEGF препарат в основном применяется в онкологии для лечения злокачественных опухолей, в офтальмологии его применение не имеет официального статуса («off-label»). Эффективности бевацизумаба в терапии влажной формы ВМД на сегодняшний день уже посвящено более 40 клинических исследований. Причем последние из них были направлены на сравнение эффекта бевацизумаба и кортикоидов ( триамцинол, дексаметазон) в лечении неоваскулярной макулодистрофии.
Пегаптаниб (Макуген, Макуджен)
Данный анти-VEGF препарат разрешен для лечения неоваскулярной ВМД в США и европейских странах. Его эффект был подтвержден рядом исследований. Согласно полученным данным, введенный в дозе 0,3 мг пегаптаниб, значимо улучшает остроту зрения, результат длиться 6 недель после инъекции. Длительный эффект достигается введением не менее трех инъекций в течение полугода.
Афлиберцепт (Айлия, Эйлеа, Eylea)
Этот препарат с самой широкой анти-VEGF активностью. Он способен воздействовать на VEGF-A, VEGF-B и PlGF. В США, он одобрен для применения в терапии влажной неоваскулярной дегенерации макулы, а также метастатических опухолей прямой кишки. Исследования афлиберцепта, как средства лечения ВМД стали проводиться позднее остальных анти-VEGF препаратов.
Среди анти-VEGF средств последнего поколения, которые только проходят необходимые исследования для последующего применения в качестве терапии макулярного отека, стоит отметить бевасираниб. Это препарат, основу которого составляют РНК, подавляет ген, синтезирующий VEGF. Он также вводится интравитреально.
Уже достаточно известен и препарат «VEGF Trap-Eye». Изначально он разрабатывался для борьбы с опухолями, но стал настоящей «ловушкой» для VEGF, ведь его молекулярное строение сходно по форме с VEGF-рецептором. При интравитреальном введении, средство нейтрализует все VEGF-A и PlGF12 изоформы.
Что такое лечение против VEGF?
Препараты против VEGF действуют в организме, блокируя выработку эндотелиального белка для роста сосудов, который стимулирует выработку кровеносных сосудов, когда это требуется организму.
Белок VEGF увеличивает его присутствие в организме, когда человек страдает от определенных заболеваний глаз, связанных с появлением новых сосудов (неоваз).
Иногда клетки могут продуцировать много белка VEGF, и, когда это происходит, существует повышенный риск аномальных кровеносных сосудов в организме. глазная структура.
Аномальные кровеносные сосуды могут значительно ухудшить зрение и зрение, что приведет к слепоте.
Какие заболевания лечит анти-VEGF?
Лечение анти-VEGF назначают в первую очередь для лечения DMAE мокрый и диабетическая ретинопатия, Оба заболевания считаются важными причинами слепоты в мире.
- La DMAE это сосудистое заболевание, которое влияет на заразаЦентральная часть сетчатка отвечает за центральное зрение и восприятие деталей. Влажная AMD — наименее распространенная форма дегенерация желтого пятна, но он является наиболее агрессивным и, следовательно, необходимо действовать быстро и с правильным лечением, чтобы остановить потеря зрения.
- La диабетическая ретинопатия Это состояние, которое возникает из-за ухудшения кровеносных сосудов, кровоснабжающих сетчатку. Когда кровеносные сосуды повреждены, существует риск утечки или разлива кровяной жидкости. Диабетическая ретинопатия вызвана высоким уровнем глюкозы в крови.
Патогенез диабетической ретинопатии
Важную роль в развитии диабетической ретинопатии играет хроническая гипергликемия. В результате этого запускается большое количество биохимических, молекулярно-генетических, патофизиологических механизмов. Все это воздействует на сосуды сетчатки и приводит к повреждению эндотелия. При этом сосудистое русло сетчатки запустевает, стенка становится более проницаемой, что вызывает гиперфильтрацию плазмы, кровоизлияния, а также гипоксию сетчатки.
В ответ на недостаток кислорода клетки сетчатки активно продуцируют специфический белок, который повышает транскрипцию гена VEGF. Это вещество влияет на эпителий, стимулирует пролиферацию и регенерацию сосудов.
Сосудистый эндотелиальный фактор роста в норме и патологии
Белок VEGF впервые был выделен еще в 1983 году. Его основной задачей было увеличение проницаемости сосудистой стенки артерий, расположенных в опухолевом узле. Белок этот относится к гликопротеинам и имеет структурные сходства с фактором роста тромбоцитов. В его составе имеется пять типов рецепторов (с тирозинкиназной активностью), то есть влияние на VEGF могут оказывать процессы эмбриогенеза, беременности, заживления раневых повреждений, рост опухолей, репродуктивная функция у женщин, развитие ишемической болезни и диабетической ретинопатии.
Белок VEGF-А изучен в наибольшей степени. У этого вещества имеется несколько изоформ, но основное влияние на клетки оно оказывает через тирозиновый рецептор, который расположен в структуре мембраны. При интравитреальном введении блокатора VEGF 165 происходит значительное замедление процессов патологической неоваскуляризации, при этом на физиологическую васкуляризацию влияние практически отсутствовало или было незначительным.
Кроме того, VEGF принимает участие в эмбриогенезе и раннем ангиогенезе. У взрослых людей в стенке сосудов эндотелиальный фактор роста действует двояко: с одной стороны, он способствует выживанию эндотелиальных клеток, с другой – стимулирует сосудистую проницаемость и вызывает расширение просвета артерий. Например, в почках VEGF контролирует работу фильтрационной системы и отвечает за гломерулогенез. Кроме того, это белок влияет на регенерацию мышечных клеток, перестройку миокарда и вызывает образование костной ткани внутри хрящей.
Помимо физиологических процессов, VEGF приводит к запуску некоторых других полезных механизмов. К ним относят рост коллатеральных сосудов в ответ на гипоксию, а также улучшение питания тканей при заживлении ран.
У пациентов с сахарным диабетом VEGF секретируется клетками пигментного эпителия сетчатки, в результате чего происходит рост новобразованнных сосудов и отек сетчатки. При сахарном диабете первого типа характерны процессы неоваскуляризации, тогда как при втором типе заболевания чаще возникает отек сетчатки, который приводит к потере центрального зрения.