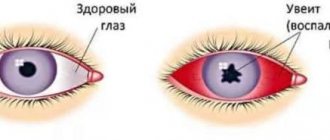
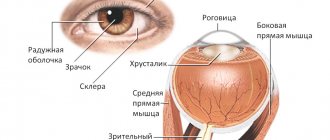
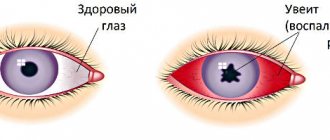
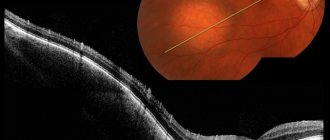
Центральный участок сетчатки (макула, или жёлтое пятно) представлен нервными волокнами и тонким слоем клеток, которые чувствительны к воздействию света и цвета (зона концентрации фоторецепторов колбочек, которые формируют центральное зрение). Благодаря наличию колбочек человек видит днём и различает цвета. Поскольку в клетках макулы содержится жёлтый пигмент, её ещё называют «жёлтым пятном». У больных, страдающих сахарным диабетом и другими общими заболеваниями, развивается макулярный отёк. Он приводит к снижению остроты или утрате зрения, в том числе – до полной слепоты.
Рис.1 Сетчатка здорового глаза и макулярный отёк на фоне диабетической ретинопатии
Причины и факторы, способствующие развитию макулярного отёка
Макулярный отёк – это не самостоятельное заболевание. Он может быть проявлением следующей патологии:
- Диабетической ретинопатии (поражения сосудов сетчатки при сахарном диабете);
- Повреждения глазного яблока или последствий оперативного вмешательства (например, удаления катаракты);
- Увеита (воспаления сосудистой оболочки глаза);
- Закупорки (окклюзии) центральной вены сетчатки (ЦВЗ) и её ветвей.
В качестве основной причины развития макулярного отёка выделяют диабетическую ретинопатию и окклюзию вен сетчатки вследствие артериальной гипертензии, атеросклероза. Реже — хирургическое воздействие или травма.
При закупорке вен сетчатки без срочного лечения может развиться необратимая потеря зрения!
Образованию макулярного отёка способствуют следующие факторы:
- Гипергликемия – повышение уровня глюкозы в крови;
- Гиперлипидемия – аномальное повышение содержания липидов и холестерина в крови;
- Чрезмерная масса тела;
- Недостаточная двигательная активность (гиподинамия);
- Возраст старше сорока или пятидесяти лет;
- Повышение внутриглазного давления, вязкости крови;
- Воспалительные заболевания других органов и систем.
Важный фактор развития макулярного отёка – врождённая и приобретенная предрасположенность к образованию тромбов. При образовании тромба нарушается ток крови по сосуду. Форменные элементы крови проникают в сетчатку, что приводит к её утолщению и отёку. В результате тромбоза вокруг поражённого участка развивается зона ишемии – «кислородного голодания».
Для того чтобы улучшился кровоток, в сетчатку из подлежащей сосудистой оболочки (хориоидеи) начинают прорастать новые сосуды с патологически утончёнными стенками. Через них жидкая часть крови (плазма) проникает в сетчатку. При повышении артериального давления аномальные стенки сосудов разрываются и кровь с форменными элементами изливается в сетчатку. Зона отёка расширяется. Макула перестаёт выполнять главную функцию – обеспечение качественного центрального зрения. Если пациенту не оказать своевременную медицинскую помощь, рецепторы сетчатки отмирают, и он может утратить зрение навсегда.
Наиболее распростространены 2 вида отёка — диабетический и кистозный. Первый развивается на фоне диабета, второй — после глазной хирургии (ещё его называют (синдром Ирвина-Гасса). Ниже мы разберём диабетический макулярный отёк (ДМО), о кистозном можно прочитать ЗДЕСЬ.
Симптомы ДМО
Диабетический макулярный отёк проявляется следующими симптомами:
- Размытым изображением в центральном поле зрения;
- Искажением изображения (прямые линии выглядят изогнутыми, волнистыми);
- Повышением чувствительности к свету.
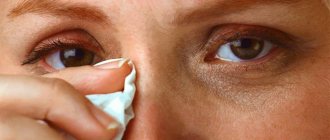
Пациенты акцентируют внимание на появление розового оттенка изображения. Они отмечают снижение остроты зрения в определённое время суток, чаще утром. Восприятие цвета может меняться в течение дня.
Рис.2 Картина зрения больного человека при отёке макулы
Диагностика
Выраженный макулярный отёк офтальмологи диагностируют во время осмотра глазного дна (процедура – офтальмоскопия). Если заболевание выявлено на этой стадии, благоприятный исход наступает далеко не всегда. Лечение проводится в течение длительного времени и требует больших усилий.
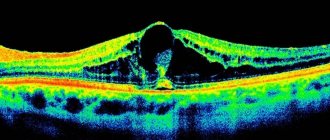
Предрасположенность к развитию заболевания или раннюю стадию патологического процесса выявляют с помощью оптической когерентной томографии (ОКТ). Такую процедуру мы рекомендуем проходить людям, у которых есть факторы, способствующие образованию тромбов вен сетчатки, 1 раз в год. Выявление макулярного отёка на ранней стадии позволяет своевременно провести экстренные мероприятия по его снятию и сохранить зрение.
Рис.3 Картина макулярноо отёка на ОКТ — оптической когерентной томографии
В нашей клинике точная диагностика заболеваний сетчатки проводится с помощью оптического когерентного томографа нового поколения DRYOCT Triton, обладающего функцией ангиографии. Он позволяет получать двухмерное и трёхмерное изображение строения сетчатки и структур диска зрительного нерва, исследовать сосуды сетчатки (при необходимости — определить место просачивания, не прибегая к введению контрастного вещества).
При применении этого метода исследования патологию макулы выявляют уже на ранних стадиях. В этом случае прогноз оптимистичный.
Опухоли орбиты
На долю новообразований орбиты приходится около 1\4 всех опухолей органа зрения. Среди них встречаются как доброкачественные (80%), так и злокачественные (20%) процессы.
В орбите могут развиваться метастатические опухоли!
Симптомы опухоли орбиты: боли в области орбиты, снижение остроты зрения и двоение, смещение и ограничение подвижности глаза, отек слизистой оболочки глаза и век, пальпируемое под кожей образование, нарушение функции век (опущение, деформация)
Следует помнить, что опухоли орбиты могут иметь бессимптомное течение
Методы диагностики патологии орбиты:
1. Офтальмологический осмотр
2. Визо-, пери-, кампи-, офтальмометрия
3. Экзофтальмометрия – неинвазивное определение степени смещения глазного яблока относительно костных стенок орбиты
4. УЗИ (в т.ч. с допплерографическим исследованием)
5. Рентгеновская компьютерная томография и магнито-резонансная томография – ведущие неинвазивные методы диагностики
6. Позитронно-эмиссионная томография
7. Биопсия – ведущий метод инвазивной диагностики опухолей орбиты. Морфологические методы диагностики новообразований орбиты: эксцизионная биопсия, инцизионная биопсия, тонкоигольная аспирационная биопсия.
Наиболее рациональный вид вмешательства определяется врачом на этапе подготовки к операции.
Только в нашем учреждении проводится современный метод диагностики – трепанобиопсия.
Хирургические методы лечение опухолей орбиты, имеющиеся в арсенале врачей-офтальмоонкологов, проводятся только в случаях отсутствия разрушений костных стенок и распространения опухоли на смежные зоны. В ином случае пациент должен быть направлен в специализированный онкологический стационар.
Виды лечения опухолей орбиты:
Зависит от клинической симптоматики, особенностей патологического процесса (предполагаемого характера новообразования, типа роста, размеров, локализации) и определяется врачом
1. Хирургическое лечение – наиболее часто применяемый вид лечения. Полное удаление образования проводится в случаях отграниченных единичных очагов в орбите
Удаление ad maximum с последующей лучевой или химиотерапией проводится в случаях диффузного роста опухоли, множественных очагов, подозрении на конкретный вид опухоли (например, лимфомы, метастазы), потребующий проведения дальнейшего химио-лучевого лечения.
Экзентерация орбиты (полное удаление мягкотканного содержимого орбиты до костных стенок) – калечащий вид операций, выполняется в случаях подтвержденного злокачественного процесса в орбите, занимающий большую часть орбиты, когда ни один другой способ лечения не показан. Возможно проведение наружного протезирования в сроки около 9-12 мес после операции.
2. Лучевая терапия — некоторые виды опухолей и воспалительных заболеваний
3. Химиотерапия – необходимость данного лечения определяется врачом-онкологом на консультации в специализированном учреждении. Необходимо, как правило, при лечении метастатических опухолей, лимфом и пр.
4. Комбинированное лечение.
5. Консервативное лечение – лечение с помощью медикаментозных средств, физиотерапии. Показано при псевдотуморозных (воспалительных) процессах, сосудистой патологии орбиты.
Состояние после курса консервативного лечения (противоотечные, сосудоукрепляющие, противовоспалительные, десенсибилизирующие ЛС).
Наблюдательная тактика возможна в случаях малого размера опухоли, предположительно доброкачественного характера, с очень медленным ростом (годами), которая не влияет на остроту зрения и косметический вид пациента.
Лечение
Лечение диабетического макулярного отёка офтальмологи часто проводят совместно с эндокринологами. Пациентам прописывают специальную диету и лекарственные средства, которые нормализуют уровень глюкозы в крови.
При консервативной (медикаментозной) терапии пациентам назначают противовоспалительные средства в виде инъекций, таблеток, капель.
Лазерная коагуляция
Самый эффективный метод избавления от большинства заболеваний сетчатки (дистрофии, разрыва, отслойки) – лазерная коагуляция, это применимо и к ДМО. Однако этот метод лечения при макулярном отёке требует острожного и взвешенного применения, поскольку лазерные лучи могут повредиться жёлтое пятно. Поэтому, коагулянты (если есть такая необходимость) наносятся по краю центральной зоны сетчатки, чтобы не допустить дальнейшего распространения отёка.
Интравитреальное введение препаратов (ИВВ)
В зависимости от причины макулярного отёка могут назначаться интравитреальные (внутриглазные) уколы различных препаратов. Такой способ доставки является наиболее эффективным при лечении заболеваний сетчатки.
Первый тип препаратов – анти-VEGF (блокаторы сосудистого фактора роста эндотелия). К ним относятся: ранибизумаб («Луцентис»), афлиберцепт («Эйлеа») и бевацизумаб («Авастин»). Последний не разрешён для применения в офтальмологии на территории России, но в некоторых клиниках используется «Off Label», т.е. не по указанным в инструкции показаниям. Анти-VEGF уменьшают отёк и препятствуют его рецидиву.
Высокой эффективностью при ДМО вызванным тромбозом вен сетчатки отличаются лекарственные препараты, которые содержат синтетические аналоги глюкокортикостероидов (гормонов, которые синтезируются корой надпочечников). Чтобы получить максимальный результат их вводят – непосредственно в стекловидное тело. Несмотря на высокую эффективность инъекций кортикостероидов по сравнению с другими фармакологическими формами (каплями, таблетками), длительность лечебного воздействия во многих случаях невысокая из-за того, что основное действующее вещество поглощается сразу.
Этого не наблюдается при имплантации в стекловидное тело инновационного препарата «Озурдекс», который сделан в виде депо-формы (импланта) и высвобождает дексаметазон дозированно – в течение нескольких месяцев.
Наша клиника имеет все возможности для лечения диабетического макулярного отёка даже в самых сложных случаях. Мы предлагаем быструю и высокоточную диагностику и возможность начать лечение (в том числе интравитреальные инъекции) у специалистов по сетчатке уже в день обращения!
Ангиоидные полосы сетчатки
- Классификация
- Диагностика
- Флюоресцентная ангиография сетчатки
- Лечение
Ангиоидные полосы сетчатки (дистрофия или синдром Гренблада-Страндберга, генерализованный эласторексис, дистрофический эластоз, эластическая псевдоксантома) – весьма своеобразная и крайне редкая форма патологии глазного дна, по виду напоминающая сосуды сетчатки. Фактически это линейные трещины, образующиеся в мембране Бруха.
Генерализованный эласторексис — это наследственное системное поражение эластической ткани кожи, сетчатки глаз и стенок кровеносных сосудов. У половины больных обнаруживаются ангиоидные полосы сетчатки глаз. У 70% больных с ангиоидными полосами сетчатки развивается потеря центрального зрения.
В 60% случаев ангиоидные полосы ассоциируются с системным эласторексисом и в этом случае носят название дистрофии Гренблада-Страндберга (или синдром Гренблада-Страндберга).
В других случаях ангиоидные полосы представляют собой самостоятельное заболевание. Возможна комбинация ангиоидных полос с серповидно-клеточной анемией и болезнью Педжета, однако сведения об этом чрезвычайно скудны.
Впервые данная нозологическая форма была описана Дойном (в 1889 г.), а несколько позднее Гренблад и Страндберг установили связь этой патологии с системным заболеванием эластической ткани — эласторексисом. В основе его лежит недостаточность образования ко-ферментов, ингибирующих эластазу.
Заболевание встречается редко и до настоящего времени недостаточно изучено. Описаны как семейные случаи заболевания, так и спорадические формы.
Заболевание носит генерализованный характер с преимущественным поражением сосудов сердца и мозга, а также желудочно-кишечного тракта, нередко с рецидивирующими, иногда профузными кровотечениями. Частое проявление заболевания – облитерирующий эндартериит. Провоцирующую роль могут играть эндокринные расстройства (сахарный диабет, поражения щитовидной железы, гипофиза), беременность, инфекционные болезни, наличие очагов хронической инфекции, токсоплазмоз, травмы.
Частота заболевания в популяции 1:160 000. Описаны 2 рецессивных и 2 доминантных типа заболевания, различающихся сопутствующими аномалиями.
- Эластическая псевдоксантома доминантная, тип 1 (177850, ген РХЕ, ВД). Клинически: утолщение кожи, кожа типа апельсиновой корки, стрии, кальцификация крупных и коронарных артерий, кровотечения из ЖКТ, кальцификация серпа твёрдой мозговой оболочки.
- Эластическая псевдоксантома доминантная, тип 2 (177860, R). Клинически: утолщённая узловатая или сетчатая кожа желтоватого цвета, участки снижения эластичности кожи, миопия, голубые склеры, высокое арковидное нёбо, встречается в 4 раза чаще, чем 1 доминантный тип. Лабораторно: эластические волокна содержат небольшие участки кальцификации.
- Эластическая псевдоксантома рецессивная, тип 1 (264800,16р13.1, ген РХЕ1, р). Клинически: симптоматика 1 доминантного типа в сочетании с кардиомиопатией и митральным стенозом. Лабораторно: фрагментация эластической ткани дермы.
- Эластическая рецессивная псевдоксантома, тип 2 (264810, р) — очень редкая форма. Клинически: кожа уплотнена, утолщена, но без стрий, сосудистые изменения отсутствуют.
Ангиоидные полосы сетчатки (АП) Дойн связывал с разрывами пигментного эпителия, Коффер (1917) — с разрывами мембраны Бруха. Электронно-микроскопические исследования показали поражение эластического слоя мембраны Бруха, набухание и расщепление эластина с последующей деструкцией и распадом. Эластические волокна превращаются в глыбки и зерна с отложением в них солей кальция, что, в конечном итоге приводит к надрывам и разрывам мембраны Бруха.
Одновременно обнаруживаются дистрофические изменения пигментного эпителия сетчатки и хориокапилляриса. Возможна отслойка пигментного эпителия экссудатом и кровью.
Локализация заболевания билатеральная с различной степенью выраженности проявлений.
Офтальмоскопически ангиоидные полосы выглядят как «сосудистые дорожки”, идущие концентрично вокруг ДЗН, образуя кольцо или полукольцо, от которого они расходятся радиально на различную протяженность, образуя своеобразное сосудистое дерево вокруг ДЗН.
Ретинальные сосуды, проходя над ангиоидными полосами, не изменяют своего хода. Цвет АП от бледно-розового до буро-коричневого, края неровные. Диаметр колеблется от 1 до 2 диаметров крупной ретинальной вены, контур слегка зазубрен.
Происхождение кровоизлияний обычно хориоидальное, реже – ретинальное, в единичных случаях может сформироваться дисковидный псевдотуморозный очаг (по типу дистрофии Кунта – Юниуса).
У лиц молодого возраста АП имеют более нежный розовый цвет и менее контрастны по отношению к основному фону глазного дна. По протяженности они, как правило, не доходят до макулярной зоны.
Зрительные функции бывают высокими, вплоть до 1,0. С возрастом АП становятся более контрастными, пигментированными, приобретая темную буровато-коричневую окраску. Отмечается постепенное увеличение их по ширине и длине, появление новых ответвлений. Изменения сетчатки и хориоидеи могут обнаруживаться не только в зоне АП, но и диффузно по всему глазному дну.
Классификация
Шульпина Н. Б. с соавт. выделяет в течении заболевания 3 стадии:
- появление стрий вокруг диска зрительного нерва;
- распространение стрий в макулярные отделы и возникновение кровоизлияний;
- процесс рубцевания с атрофией хориоидеи и отложением глыбок пигмента.
Мизгиревой А. П. выделены 2 типа изменений центральной зоны:
- очагово-диффузная хориоретинальная дистрофия, протекающая по сухому типу (неосложненная форма); Медленно прогрессирующая атрофия хориокапиллярного слоя, а также вторичные изменения пигментного эпителия и наружных слоев сетчатки. Кровоизлияний и отека в макулярной области у больных этой группы не было, зрительные функции сохранялись довольно высокими.
- хориоретинальная дистрофия, протекающая по «влажному типу” (осложненная форма). Формирование субретинальной неоваскулярной мембраны (СНМ). Клиническая картина у этих больных определялась разрушением мембраны Бруха и прорастанием новообразованных сосудов с последующими рецидивирующими кровоизлияниями и отеком с отслойкой пигментного эпителия и нейроэпителия,. Новообразованные сосуды происходили из хориокапилляриса и имели капиллярный тип строения. Прорастая стекловидную пластинку, они появлялись вначале в наружных слоях сетчатки, затем во внутренних. Отек носил транссудативный характер, происходил из хориокапилляриса и новообразованных сосудов. Кровоизлияния имели такой же генез. Ретинальные сосуды, как правило, оставались интактными, т.е. развивалась СНМ. ФАГ у этих больных была типична для СНМ в зависимости от степени ее проявления. Лишь в трети случаев СНМ тесно связана с АП, дистальный конец которых переходит в гиперфлюоресцеирующую зону СНМ. Однако иногда даже ангиографически не выявляются признаки наличия АП рядом с зоной формирования СНМ. Зрительные функции, как правило, низкие. Наблюдается рецидивирующий характер течения. Каждое обострение сопровождается развитием глиальных элементов с последующим формированием глиальных очагов, которые могут занимать всю макулярную область и проминировать, имея вид псевдотуморозных образований. Впоследствии в центре образуется рубец, захватывающий область фовеолы, что значительно снижает центральную остроту зрения.
Отмечается, что 1 тип макулярных изменений с возрастом может переходить в 2, причем в отдельных случаях с большой долей вероятности провоцирующим фактором можно считать контузию глаза, после которой процесс протекал уже как 2 тип.
Диагностика
Диагноз основывается на клинической картине; в сомнительных случаях проводят гистологическое исследование пораженной кожи (очаги дистрофии и распада эластических волокон дермы и их инфильтрация солями кальция).
Флюоресцентная ангиография сетчатки
В хориоидальную или раннюю артериальную фазы обнаруживаются гиперфлюоресцеирующие с неровными, но четкими контурами дорожки; пик гиперфлюоресценции совпадает с артерио-венозной фазой и держится долго, постепенно ослабевая к концу исследования.
Временные параметры артериальной и венозной фаз ретинального кровообращения, а также время артериальной и венозной перфузии могут быть в норме, но, как правило, отмечается удлинение ранней венозной фазы и венозной перфузии.
При неосложненных формах экстравазации флюоресцеина из ретинальных сосудов нет. В целом ангиографическая картина глазного дна при наличии ангиоидных полос очень наглядна и специфична для данной патологии.
Лечение
Лечение АП не разработано и, по мнению некоторых авторов (Шульпина Н. Б. с соавт.), неэффективно. Отмечен положительный клинический эффект от применения АКТГ и преднизолона.
Рекомендуются антиоксиданты (эмоксипин, токоферол), парабульбарное введение этамзилата, электрофорез цистеина и 3% йодистого калия, а также аргонлазеркоагуляция трещин мембраны Бруха.
При появлении геморрагий применяют гемостатические, противоотечные и рассасывающие средства.
Необходима профилактика атеросклеротических изменений, ухудшающих течение основного процесса.
Больные должны находиться под диспансерным наблюдением дерматолога, окулиста, терапевта.